未来医療を実現する医療機器・システム研究開発事業
(医療機器等に関する開発ガイドライン(手引き)策定事業)
超高齢社会を迎えたわが国において、「国民の長寿」と「質の高い生活」を実現するためには、新しい医療機器・再生医療等製品の開発と医療現場への円滑な導入が不可欠です。この分野の活性化・国際競争力の強化を図り、迅速な開発と審査を実現し、また、産業の育成の観点から、医療機器・再生医療等製品及びこれらに関連する研究開発の指針を明確化することが必要と考えます。
これらの目的のために、平成17年度から経済産業省に「医療機器開発ガイドライン評価検討委員会」と厚生労働省に「次世代医療機器・再生医療等製品評価指標検討会」が設置[PDF:87KB]され、以降、これらの検討会の連携(合同検討会)によって、新しい医療機器等の開発促進及び迅速な薬事承認審査に活用できる開発ガイドライン及び評価指標が策定されております。
これまで策定した開発ガイドラインは経済産業省のホームページをご参照ください。機器の開発、薬事申請などにご活用ください。
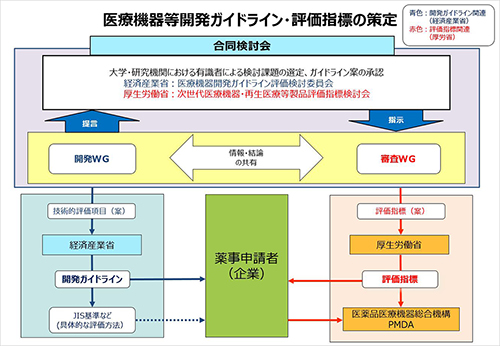
(図をクリックすると大きな図を参照できます)
産業技術総合研究所では、日本医療研究開発機構より「医療機器等に関する開発ガイドライン(手引き)策定事業」を受託し、医療機器等に関連する技術分野ごとに医学系学会、工学系学会および関連企業からの専門家によって構成する開発ワーキンググループ等を組織・運営し、医療機器等開発における問題点の抽出と内容の分析、諸外国における医療機器に関する標準やガイドラインの調査も併せて実施いたしました。
今年度は7課題に関して審議し、5件の開発ガイドライン(「再生医療等製品の製造におけるチェンジオーバー」、「精密積層造形技術を用いた人工股関節寛骨臼コンポーネント」、「近赤外イメージング検査システム」、「医用画像診断支援システム(人工知能技術を利用するものを含む)」、「ホウ素中性子捕捉療法(BNCT)」を提案するに至りました。
ワーキンググループにおける審議の過程、調査結果などを以下の報告書にまとめました。
|
|
※報告書内にあるガイドラインは、(案)となっております。正式なガイドラインは経済産業省のHPに公表されます。
|
本事業では、これまでに59件(改定版を含む)の開発ガイドラインを策定いたしました。
また、「次世代医療機器・再生医療等製品評価指標検討会」において、迅速な審査に必要な評価指標に関して検討がなされております。国立医薬品食品衛生研究所が事務局となり、審査ワーキンググループを設置して審査の迅速化という観点から種々の検討が進められております。同研究所のホームページに掲載される審査ワーキンググループの報告書(https://dmd.nihs.go.jp/jisedai/)も併せてご覧ください
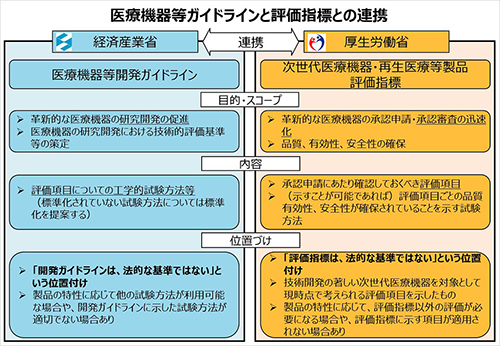
(図をクリックすると大きな図を参照できます)
関連リンク