国立研究開発法人 産業技術総合研究所【理事長 中鉢 良治】(以下「産総研」という)創薬基盤研究部門【研究部門長 織田 雅直】舘野 浩章 主任研究員、平林 淳 首席研究員、幹細胞工学研究グループ 小沼 泰子 主任研究員、伊藤 弓弦 研究グループ長は、和光純薬工業株式会社【代表取締役社長 小畠 伸三】(以下「和光純薬工業」という)試薬化成品事業部 開発第一本部 ライフサイエンス研究所と共同で、移植用細胞から腫瘍を引き起こすヒトiPS細胞やヒトES細胞(以下「ヒトiPS/ES細胞」という)を除く技術を開発した。
ヒトiPS/ES細胞から分化させて作製した移植用細胞には、ヒトiPS/ES細胞が残存し腫瘍化する可能性があり、再生医療に応用する際の大きな障壁となっている。今回開発した技術により、移植用細胞に残存するヒトiPS/ES細胞を効率的に除去できることから、ヒトiPS/ES細胞から作製した移植用細胞を用いた再生医療の安全性向上への貢献が期待される。
なお、この技術の詳細は、2015年4月9日(米国東部時間)に米国科学誌Stem Cell Reportsにオンライン掲載される。
 |
|
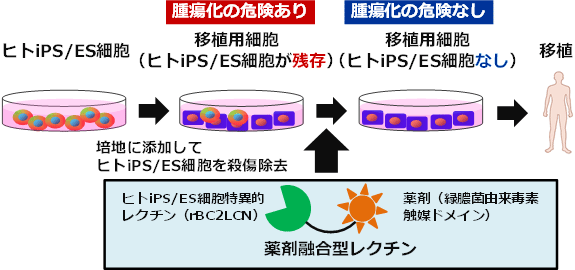
移植用細胞から腫瘍を引き起こすヒトiPS/ES細胞を除く技術の概要 |
ヒトiPS/ES細胞は無限に増殖できる能力(自己複製能)や、心筋細胞や神経細胞など、あらゆる細胞に分化する能力(多能性)を持つ。そのため、ヒトiPS/ES細胞は各種の疾病を根本的に治癒する再生医療のための細胞源として社会的にも大きな期待が寄せられている。しかし、全てのヒトiPS/ES細胞を目的の細胞に分化させることは困難であり、一定数の未分化な状態のヒトiPS/ES細胞が残存してしまう場合がある。ヒトiPS/ES細胞を患者に移植した場合には腫瘍を形成してしまう可能性があるため、移植用細胞に残存するヒトiPS/ES細胞を除去する必要がある。しかし、従来の一般的な技術では移植用細胞を前もって1つ1つの細胞に解離してからセルソーターという特殊な装置を用いてヒトiPS/ES細胞を取り除くため、細胞シートなどへの適用ができない、処理速度が遅い、移植用細胞の生存に悪影響を与える可能性がある、などの課題がある。このような課題を解決するために、移植用細胞に残存するヒトiPS/ES細胞を、安全、確実、かつ簡便に除去できる技術が求められている。
産総研は、細胞表面を高密度に覆う糖鎖を迅速、高感度に解析する技術としてレクチンマイクロアレイを開発してきた。特に近年はレクチンマイクロアレイを活用して、ヒトiPS/ES細胞表面糖鎖を網羅的に解析することにより、幹細胞の品質評価・選別技術の開発に取り組んできた(2011年6月22日 産総研主な研究成果)。その結果、レクチン(糖結合タンパク質の総称)の一種であるrBC2LCNがヒトiPS/ES細胞に特異的に結合することを見いだし、和光純薬工業との共同研究により、rBC2LCNを用いてヒトiPS/ES細胞を生きたまま染色できる試薬を開発した。また、ヒトiPS/ES細胞への結合機構を解析したところ、rBC2LCNはポドカリキシンという糖タンパク質上の特定のO型糖鎖に結合することを明らかにした(2013年3月19日 産総研プレス発表)。さらに、さまざまな種類のヒトiPS/ES細胞からポドカリキシンが培養液中にも分泌されているという現象を見いだし、これを利用して細胞培養液を用いて移植用細胞に残存するヒトiPS/ES細胞を簡便に測定する技術を開発してきた(2014年2月17日 産総研主な研究成果)。
なお、本研究開発は、和光純薬工業からの資金提供型共同研究(平成23年度~)により産総研と和光純薬工業が共同で実施した。
今回、rBC2LCNがヒトiPS/ES細胞に結合した後に、細胞内に取り込まれるという現象を見いだした。そこで細胞内に取り込まれるとタンパク質合成を阻害し細胞死を引き起こす緑膿菌由来外毒素をrBC2LCNのC末端部分に融合させた組換えタンパク質(薬剤融合型レクチン)を考案した。
精製した薬剤融合型レクチンをヒトiPS細胞に24時間反応させた後の顕微鏡写真像を図1に示す。生きた細胞を細胞質が緑色蛍光、死んだ細胞を核が赤色蛍光で染色処理し観察すると、薬剤融合型レクチンを培養液に添加していない(0 µg/mL)場合は、多くのヒトiPS細胞は培養皿に接着し、緑色蛍光で染色されたものの、赤色蛍光ではほとんど染色されなかった。つまりほとんどのヒトiPS細胞が生きていることを示している。
一方、10 µg/mLの薬剤融合型レクチンを培養液に添加した場合、ほとんどの細胞が培養皿への接着能力を失い、培養液中に浮遊した。わずかに接着している細胞も、死んだ細胞だけが染色される赤色蛍光で染色された。つまり、ほとんどのヒトiPS細胞が死んだことを示している。薬剤融合型レクチンはヒトES細胞でも同様の効果を示した。これらの結果から、今回開発した薬剤融合型レクチンを用いると、分化していない各種ヒトiPS/ES細胞を効率的に除去できることが分かった。
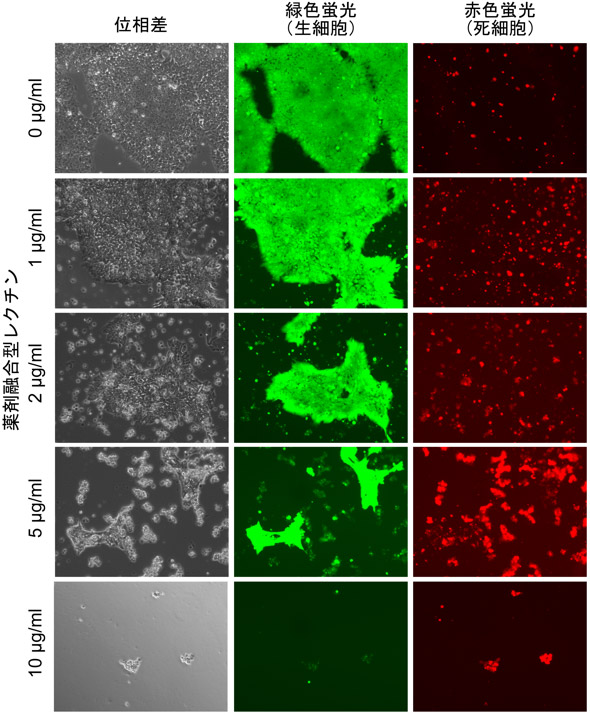 |
図1 薬剤融合型レクチンのヒトiPS細胞への効果
位相差:実際の細胞の形態、緑色蛍光:生細胞が緑色に染色、赤色蛍光:死細胞が赤色に染色 |
分化した細胞への影響を調べるため、薬剤融合型レクチン(10 µg/mL)を、レチノイン酸(RA)で分化させたヒトiPS細胞、皮膚繊維芽細胞、脂肪由来間葉系幹細胞に作用させた。その結果、ほぼ全ての細胞が緑色蛍光で染色されたものの、赤色蛍光ではほとんど染色されなかった。つまり、これら分化細胞は生きていることを示している(図2)。すなわち、薬剤融合型レクチンは、未分化なヒトiPS/ES細胞を選択的に除去し、分化した体細胞の増殖や生存には影響を与えないことが分かった。
薬剤融合型レクチンは、細胞をあらかじめ分離するといった前処理も必要なく、細胞培養液に添加するだけで、培養している分化した細胞に影響を与えずに、未分化ヒトiPS/ES細胞だけを選択的に除去でき、大量の細胞や細胞シートなどへの適用も可能である。再生医療に用いる移植用細胞の製造や、創薬スクリーニングのための細胞調製など、さまざまな用途への応用が期待される。
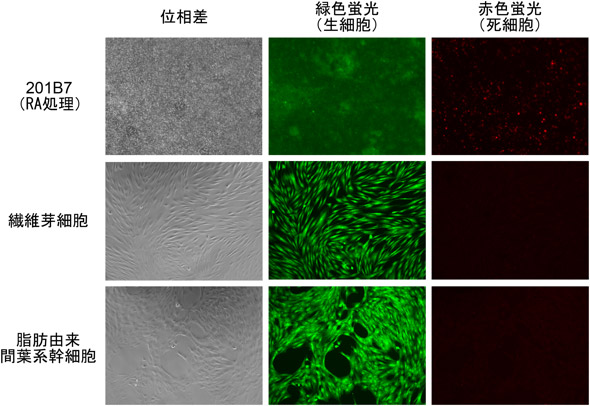 |
図2 薬剤融合型レクチンの分化細胞への効果
位相差:実際の細胞の形態、緑色蛍光:生細胞が緑色に染色、赤色蛍光:死細胞が赤色に染色 |
薬剤融合型レクチンはヒトiPS/ES細胞を除去するための試薬として1年以内に実用化される予定である。また、今後は再生医療に用いるヒトiPS細胞由来の心筋細胞や神経細胞などの細胞製造への適用性を検証することにより、ヒトiPS/ES細胞から作製した移植用細胞を用いた再生医療の安全性向上に貢献していく予定である。