国立大学法人 名古屋大学【総長 平野 眞一】(以下「名古屋大学」という)大学院工学研究科【研究科長 小野木 克明】マイクロ・ナノシステム工学専攻 福田 敏男 教授の研究グループと、国立大学法人 東北大学【総長 井上 明久】(以下「東北大学」という)大学院工学研究科【研究科長 内田 龍男】バイオロボティクス専攻 新井 史人 教授、および独立行政法人 産業技術総合研究所【理事長 吉川 弘之】(以下「産総研」という)界面ナノアーキテクトニクス研究センター 清水 敏美 研究センター長と高軸比ナノ構造組織化研究チームは共同で、有機ナノチューブ(以下「ONT」という)をナノ流路として用いた1フェムトリットル(フェムトは千兆分の1、10-15)以下の溶液噴出が可能と考えられるナノピペット(以下「ONTナノピペット」という)を開発した。
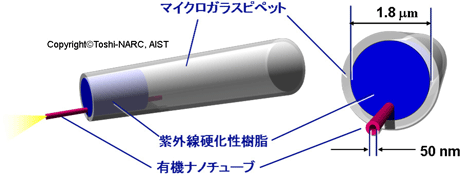
ONTナノピペットは、ナノ流路となる一本の有機ナノチューブ(内径50 nm、外径400 nm、長さは約10 µm)をマイクロガラスピペット(先端内径1.8 µm=1,800 nm)にマイクロマニピュレーション技術を駆使して取り付け、紫外線硬化性樹脂で隙間を埋めたものである(図1)。このピペットは噴出のための印加電圧を変化させることで噴出量を制御できる。今後、単一の細胞(容量は約1,000フェムトリットル)内への超極微量の有用物質注入による医療応用、あるいは超極微量の成分吸引による単一細胞分析などへの活用が期待できる。
本研究成果は、2007年8月2日~5日に香港で開催される米国電気電子学会主催のThe 7th IEEE International Conference on Nanotechnology (IEEE-NANO 2007)で発表される。
|
(a) |
|
(b) |
|
|
|
 |
|
図1 作製したONTナノピペットの(a)光学顕微鏡写真と(b)その構成イメージ図
|
生体分子の分離分析に使われる中空シリンダー容器の大きさは歴史的に、内径数cmのカラムクロマトグラフィー用ガラスカラムから、内径数mmの高速液体クロマトグラフィー用ステンレスカラムへ、さらに、内径100 µm(1 µmは百万分の1メートル)のガラスキャピラリーやマイクロチップデバイスへ、といったようにサイズの微小化が進んでいる(図2)。それら中空シリンダー状の微小空間に閉じ込められる分子の数は極少数となり、現在ではマイクロチップデバイスを用いて108~1010個の分子を分析することが可能となっている。106個以下のさらに少数の分子を分析、あるいは取り扱うためには、さらに内径の小さい中空シリンダー容器の作製が不可欠である。しかし、既存の微細加工技術では最小加工寸法が数十nmと言われ、分析デバイスでは内径1 µm以下の中空シリンダー構造を直接微細加工するには限界があり、ブレークスルーとなる革新的手法の確立が求められている。
現在、ガラスピペットの先端を最小で内径数十 nm程度に加工することは可能であるが、加工精度やピペットの操作性(先端の位置決め)等の点において大きな問題を抱えている。また、これまでにナノピペットの作製例としては(1)磁力を利用して磁気を帯びたカーボンナノチューブをマイクロガラスピペット先端に固定して作製した例、(2)マイクロガラスピペットの先端に集束イオンビームによる表面励起反応を用いてノズルを堆積した例、(3)ホウケイ酸塩ガラス管を引き延ばして作製した例がある。しかしながら(1)では多数の噴出孔ができる可能性があり、また毛細管現象による吸い込みは実証されているが、溶液の噴出は記述されていない、(2)では作製時間が長い上に、高度なシステムが必要である、(3)では形状制御が困難であり、先端が長いために光学顕微鏡観察下での分解能限界や振動などの問題がある、といった欠点がある。
これらの欠点を解決した、形状制御性、操作性、超極微量の溶液噴出性に優れたナノピペットを特別な装置を使わず容易に作製する手法が望まれていた。そこで、分子の自己組織化技術で作製した内径100 nm以下の中空シリンダー状構造体(有機ナノチューブ)を“マイクロ構造”に組み込み固定する技術の開発に取り組んだ。
|
|
|
図2 分離分析用の中空シリンダー容器の微細化年代推移 |
産総研界面ナノアーキテクトニクス研究センターでは、数ナノメートル程度のサイズ分解能を有する分析デバイスを作製するために、微細加工技術(トップダウン手法)などで作製されたマイクロチップやマイクロキャピラリーに、自己組織化技術(ボトムアップ手法)で作製した有機ナノチューブやナノ粒子を固定する技術の確立を目指してきた。一方、名古屋大学と東北大学では、レーザー操作による単一細胞マニピュレーション法や光ピンセットを用いた極微小物体の3次元6自由度の制御法などを開発してきた。
今回、産総研が開発した分子の自己組織化技術で得られた有機ナノチューブ構造体を、名古屋大学と東北大学で開発したマイクロマニュピレーター用ステージを実体顕微鏡下に取り付けた3次元マニピュレーション技術と融合させることにより、ナノピペット作製を目指した。
なお、本研究のうち、名古屋大学と東北大学の開発した3次元マニピュレーション技術については、文部科学省の科学研究費補助金の助成を得たものである。また、産総研では、過去10年にわたってナノチューブ形成用両親媒性分子の設計、合成、自己集合化の研究開発を行ってきたが、今回の研究については、独立行政法人 科学技術振興機構【戦略的創造研究推進事業発展研究(SORST)プロジェクト、平成17~20年度】の一部として実施したものである。
今回開発したONTナノピペットとは、束状になっていない一本の有機ナノチューブ(内径50 nm、外径400 nm、長さは約10 µm)をマイクロマニピュレーション技術により、マイクロガラスピペットの先端(内径1.8 µm)に取り付けて、紫外線硬化性樹脂で有機ナノチューブとマイクロガラスピペットの隙間を埋めたもので、有機ナノチューブをナノ流路として利用している(図3)。このONTナノピペットは(1)通常のマイクロガラスピペットと同様に操作、観察が可能である、(2)マイクロガラスピペットの位置そのものがナノピペットの先端位置であり焦点合わせが容易である、(3)マイクロガラスピペットのマイクロスケールの先端径と、有機ナノチューブのナノスケールの噴出口が両立しているため、形状的に強度に優れる、(4)それと同時に振動などの問題が生じる可能性が低減される、といった利点をもち、従来研究の問題点を解決している。有機ナノチューブの先端直径が均一であるため、ナノピペットの構造の制御性にも優れている。
また、作製には、ごく一般的な微動ステージを用いたマイクロマニピュレーターと光学顕微鏡を使用するだけで、高価で大型の特別な装置を全く必要としないことも本手法の特徴である。
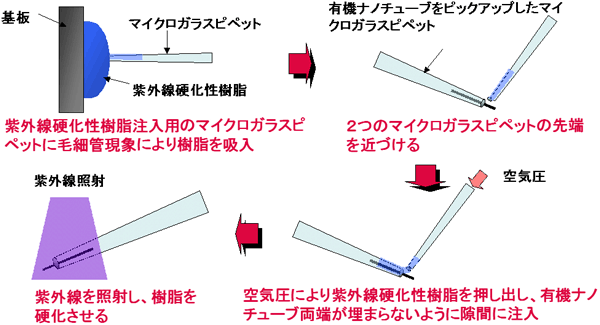
作製工程は、全て光学顕微鏡で観察しながら、マイクロマニピュレーション技術を用いて行う(図4)。工程は、大きく分けて有機ナノチューブのピックアップ工程とシーリング工程の二つの操作から構成される。ピックアップ工程とは、マイクロガラスピペット内壁に有機ナノチューブをピックアップする手法(図4(1))であり、シーリング工程とは、紫外線硬化性樹脂を用いて、有機ナノチューブを固定するとともに、マイクロガラスピペットとの間の隙間を密閉する手法である(図4(2))。
|
(1)ピックアップ工程 |
|
|
|
|
|
(2)シーリング工程 |
 |
|
図4 ONTナノピペット作製のための工程概略図 |
実際に作製したONTナノピペットの光学顕微鏡写真は、図1(a)に示したが、このようにマイクロスケールの先端径(1.8 µm)とナノスケールの噴出口(50 nm)を組み合わせたナノピペットが作製できた。また、ナノピペットとしての有用性を確認するために、蛍光物質であるローダミン6Gを含む蛍光溶液の噴出実験を行った。電気的な泳動力により溶液を噴出させ、倒立型光学顕微鏡の暗視野蛍光像により観察した(図5)。電圧300 V以上から噴出を確認することができ、噴出量は電圧の増加に伴い徐々に増加している。また、従来の内径約1 µmのマイクロガラスピペット(図5(1))とONTナノピペット(図5(2))の蛍光溶液の噴出量にも大きな差が見られる。この結果から、ONTナノピペットからの噴出量は電圧により制御可能であり、市販の500 nm径のマイクロガラスピペットと比較して、百分の1~一万分の1量に相当する超極微量(1フェムトリットル以下)の溶液噴出が可能であると考えられる。予備実験として、有機ナノチューブを用いずにマイクロガラスピペット先端を紫外線硬化性樹脂で埋めたピペットを用いて同様な溶液噴出実験を行った結果、全く蛍光溶液の噴出現象は観察できなかった。
|
|
|
図5 (1) 内径約1 µmのマイクロガラスピペットから、(2)(b)~(g)はONTナノピペット(印加電圧を526 Vまで変化)からの蛍光溶液噴出挙動の相違(光学顕微鏡の暗視野蛍光像) |
ONTナノピペットを光学顕微鏡下マイクロマニピュレーションシステムに組み込むことにより、単一細胞(容量約1,000フェムトリットル)内への1フェムトリットル以下の有用物質の溶液注入や、1フェムトリットル以下の成分吸引など、局所環境制御用ツールとして、生物学分野に応用することを考えている。そのために、ナノピペット先端素材として弾力性のすぐれた各種の内径と制御された内径サイズをもつ有機ナノチューブの合成法開発、注入用溶液の条件、噴出した溶液の拡散の制御、電気的な泳動力を効果的に発揮する電極のパターン開発などが重要な要素技術であると考えられる。さらに、ボトムアップ手法(自己組織化技術)とトップダウン手法(微細加工技術)の融合技術を構築するために、ナノチューブなどのナノ構造をマイクロ構造の中や上に組織化する手法を通して、ナノバイオテクノロジーに寄与する研究開発を進めていく。