ナガセダイアグノスティックスと産総研がスマートセル技術の実用化に成功!
ナガセダイアグノスティックスと産総研がスマートセル技術の実用化に成功!

2025/07/31
初回掲載日 2024/10/09
ナガセダイアグノスティックスと産総研がスマートセル技術の実用化に成功!検査試薬原料コレステロールエステラーゼの大量生産に至るまで

 健康診断の際に測定されるコレステロール値、血糖値、尿酸値などの診断には、生化学検査試薬などの臨床検査薬(体外診断用医薬品)が用いられる。ナガセダイアグノスティックス株式会社*1は、これら検査薬の原料となる酵素生産において高い国内シェアを持つ。同社と産総研は、「スマートセル技術」の実用化により、コレステロール値の測定に使われる酵素「コレステロールエステラーゼ」の大量生産と製品化に成功した(2023/6/30プレスリリース記事)。この成果は、両者が細胞の物質生産の仕組みに関する知見、ゲノム解析、ゲノム編集技術などを集結させながら、いくつもの失敗を乗り越えて手にしたものだ。バイオエコノミー社会の発展へ寄与するこの技術の開発に携わった診断薬事業部のメンバーと産総研の研究者へのインタビューを通して、両者の挑戦の軌跡をたどった。
健康診断の際に測定されるコレステロール値、血糖値、尿酸値などの診断には、生化学検査試薬などの臨床検査薬(体外診断用医薬品)が用いられる。ナガセダイアグノスティックス株式会社*1は、これら検査薬の原料となる酵素生産において高い国内シェアを持つ。同社と産総研は、「スマートセル技術」の実用化により、コレステロール値の測定に使われる酵素「コレステロールエステラーゼ」の大量生産と製品化に成功した(2023/6/30プレスリリース記事)。この成果は、両者が細胞の物質生産の仕組みに関する知見、ゲノム解析、ゲノム編集技術などを集結させながら、いくつもの失敗を乗り越えて手にしたものだ。バイオエコノミー社会の発展へ寄与するこの技術の開発に携わった診断薬事業部のメンバーと産総研の研究者へのインタビューを通して、両者の挑戦の軌跡をたどった。
高生産性を追求し、失敗を乗り越え、スマートセルにたどり着く
健康診断で測定されるコレステロール値。この検査に使われる試薬の原料が「コレステロールエステラーゼ(以下、CE)」と呼ばれる、コレステロールエステルを分解する酵素だ。採取した血液成分にこの酵素を加えて反応させ、色素の変化を数値化することで、血中のコレステロール値の高低を測ることができる。1970年代初頭からこの酵素を検査薬原料として供給してきたのが、2025年7月よりナガセダイアグノスティックス株式会社*1として営業を開始した、旭化成ファーマ株式会社診断薬事業部(当時)だ。
CEは自然界に存在する微生物「バークホルデリア・スタビリス」から複雑な経路を経て細胞外に分泌されることが以前から知られており、従来はこの菌そのものを培養タンクで培養することで、CEを生産していた。しかし生活習慣病が社会問題化し、コレステロール値に対する人々の関心が高まることにより、検査試薬の需要が年々増加。2000年代に入る頃にはCEを効率よく増産することが、診断薬事業部の重要課題の一つとなっていた。
「診断薬原料の酵素生産において、当社は国内のリーディングカンパニーです。CEの市場シェアを保ちながらコストダウンを図り、事業をさらに拡大することが診断薬事業部の重要課題となっていました」と、ナガセダイアグノスティックス株式会社診断薬事業部開発研究部の村松周治主幹研究員は背景を語る。
タンパク質や酵素の生産効率を高めるためには、遺伝子組換えを行った大腸菌を用いてタンパク質生産を行う方法や、生産菌自体の遺伝子を変異させて生産量を上げる手法(突然変異育種法)などが一般的に用いられる。ただ、CEに関してはこういった手法を用いても期待するレベルの生産効率の向上は達成できなかった。例えば突然変異育種法では、野生株の約2.8倍までは生産量が向上したが、そこで頭打ちになってしまったのだ。
「2年間ほど、当時使われていたあらゆる方法を試しましたが、うまくいかない。いったんは研究が中断しましたが、再び動き出したのは、2016年度に始まったNEDOのプロジェクトへの応募がきっかけでした」と振り返るのは、現在はナガセダイアグノスティックス株式会社酵素製品部営業課で体外診断用酵素製品の普及促進を担う小西健司マネージャーだ。
このプロジェクトは「スマートセルプロジェクト*2」と呼ばれる。生物の細胞を人工的に改変して、スマート(性能が高い)セル(細胞)をつくり出し、酵素やタンパク質の生産能力を高めて、それを原料に工業製品の素材や医薬品をつくるという試みだ(産総研マガジン「スマートセルとは?」)。
産総研の生命工学領域の研究者たちは、以前から共同研究で成功実績のあった診断薬事業部に、「なにか新しいテーマで共同提案しないか」と誘いをかけた。その誘いを受けたのが、当時、旭化成ファーマ診断薬事業部の酵素開発部門を率いていた酒瀬川信一だ(酒瀬川はのちに、産総研に所属を移し現在はバイオものづくり研究センター総括研究主幹を務めている)。
「『絶対無理なテーマならありますが……やりますか?』と悩みながらも応じました。産総研とは、共同研究で成功実績があります。今回のプロジェクトは確かに難しいけれど、この内容が実現すれば大きなインパクトがある、そう判断して、プロジェクトへの参画を決めました」と、酒瀬川は言う。

野生株を宿主とするコレステロールエステラーゼ組換え発現技術を世界で初めて確立
スマートセル開発においては、まず微生物のゲノム情報を取得する必要がある。バークホルデリア・スタビリスは3つの環状染色体の中に、6,764個の遺伝子を持つことがわかった。
研究チームは、大腸菌を用いてタンパク質生産を行う方法ではなく、バークホルデリア・スタビリスそのものを宿主とした組換え発現系の構築を目指した。それは、過去に小西たちが積み重ねてきた大腸菌を使う実験により、「大腸菌では原理的にCEの生産量は向上しない」という知見があったからだ。
まずは、CEを高発現させる新規プロモーター*3を探索した。複数の条件で培養した菌体からRNAを抽出し、シーケンス解析により各遺伝子の転写量を算出。ここで得られた各遺伝子の転写量情報を基に、培養条件の変化に影響されず、構成的に遺伝子を強く発現制御する最適プロモーター配列を把握することに成功した。
それらを使った結果、バークホルデリア・スタビリスそのものを宿主とした発現系の構築には成功したが、事業化にはまだ生産効率が低く、短時間にCEの生産量を上げることはできなかった。さらに、従来手法や遺伝子情報解析を活用した手法を用い、作製した多数の変異株の中から生産効率の高い株を探索したが、CE生産効率の向上に寄与する遺伝子を見いだすことはできず、十分なCE生産量を得られる株はみつけられなかった。
研究はいったん頓挫するかに見えたが、プロジェクトメンバーらは、まだあきらめなかった。4,000以上の変異株の中から比較的生産量の高かった数株を選び出し、さらに組換え発現系を構築する際に得た発現ベクターを、この数株に導入してみたところ、CE生産量が顕著に向上した株を発見することができた。
「それまでの実験の5倍ほどの高い活性を示したので、すごく驚きました。最初に発見した時は、『絶対ウソだ……。もしかして私が実験プロセスを間違ったんじゃないかな』と思ったほどです」と振り返るのは、ナガセダイアグノスティックス株式会社診断薬事業部開発研究部の村田里美研究員だ。
新たに発見したこの高生産株には、不思議なことに本来3つある染色体のうち第3染色体がすべて欠損していることがわかった。後に判明するのだが、その欠損した第3染色体上に、生産能力を高めるための鍵を握る複合体を構成する3つの遺伝子が存在していた。第3染色体上の3つの遺伝子のいずれかが破壊されることで発現ベクターの安定性が向上し、培養後期まで転写が継続するというメカニズムだったのだ。
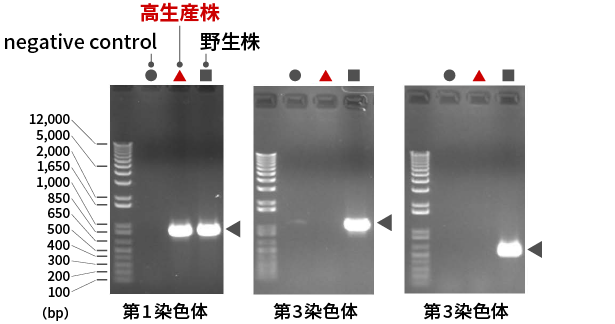 高生産株のゲノムを調べた実験結果。第3染色体の異なる2つの領域で増幅が確認できず、第3染色体自体が欠損していると考えられた。
高生産株のゲノムを調べた実験結果。第3染色体の異なる2つの領域で増幅が確認できず、第3染色体自体が欠損していると考えられた。
この研究成果を受けて、カギを握る遺伝子を特定し、詳細なメカニズムを解明するため、さらに研究を進めた。
新型コロナウイルス感染症が広がる以前は主に、札幌にある産総研北海道センターへ、静岡県伊豆の国市から診断薬事業部の研究者が訪れ、関係者がリアルで集まる定例会議が2週間おきに続けられていた。「前回よりは、少しでもいい結果を出さないといけない。これは双方にとってプレッシャーでした」と、小西は振り返る。
試行錯誤を重ねながら、第3染色体上でCEの生産効率が向上するメカニズムを担う原因遺伝子の特定を進めた。気の遠くなるような数の遺伝子変異導入をこなし、最終的に高生産株の第3染色体上で特異的に遺伝子が変異している箇所を同定した。野生株からそれらの遺伝子を破壊すると、CEの生産性が上がることを確認し、宿主のバークホルデリア・スタビリス側でCE発現を抑制する要素を特定することに成功した。この成果を元に、先に発見していた最適プロモーター配列を用いて構築した発現ベクターを、発見した高生産性株に導入してCE活性を測定すると、異様に高い活性を示した。
そして2021年、最適プロモーター配列と改変型バークホルデリア・スタビリス宿主を組み合わせることで、CEの生産能力を野生株の30倍以上に引き上げた「バークホルデリア・スタビリススマートセル」の技術開発に、世界で初めて成功したのだ。
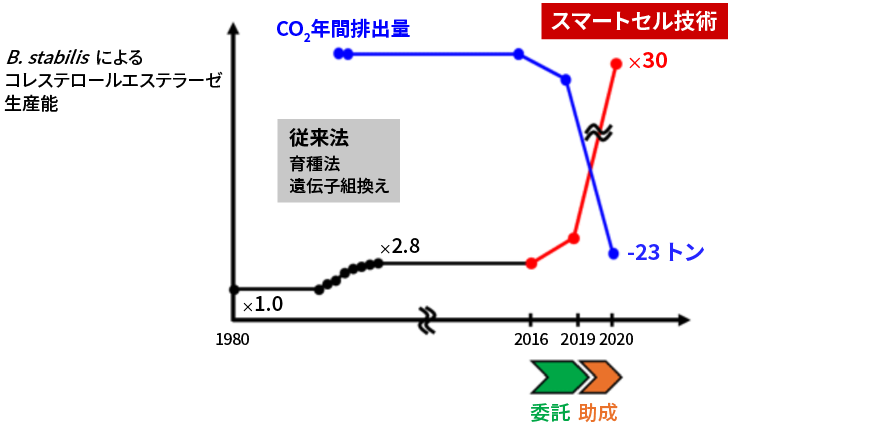 スマートセル技術の適用によって、CE生産能が30倍に向上。効率化によってCO2排出量の削減にもつながった。
スマートセル技術の適用によって、CE生産能が30倍に向上。効率化によってCO2排出量の削減にもつながった。
量産化に立ちはだかる壁を超えて製品発売へ
「ナガセダイアグノスティックスの研究者たちは、あらゆる可能性を念頭にひたむきに試すという研究姿勢を持たれています。最初の高生産性株の発見は偶然だったにしても、途方もない数の試行錯誤の過程が偶然を呼び寄せた――ある意味、必然だったのかもしれません」と、プロジェクトメンバーの粘り強い研究姿勢を評価するのは、産総研バイオものづくり研究センター応用機能分子デザイン研究チームの安武義晃主任研究員だ。
一方の産総研も、このプロジェクトでは通常は用いない技術を提案、あえて挑戦している。大腸菌ではなく、バークホルデリア・スタビリス自体を宿主とした組換え発現系を選択したことも、その一つだ。
「大腸菌による組換えはすでに多くの知見が蓄積していて、実験ツールもたくさんの種類があるので、一般的にはまずそれらを試すものです。しかし、バークホルデリア・スタビリス自体を宿主とするという方法は、そのためのツールがそろっていないし、日和見菌として知られる菌株でもあるため、ラボでの扱いにも注意が必要になる。ただ、私たちはそうした新規領域でのツール開発の経験と自負があったので大腸菌に頼らず、あえてそれを推し進めました」と、安武は語る。
4年にわたるNEDOプロジェクトを経て、CEの量産化にも成功した。この量産プロセスで生産したCE製品(製品名:CEN II)は、脂質異常症検査薬の原料として2023年6月から販売が開始されている。NEDOプロジェクトの成果が比較的短期間で製品化に直結した、希有な事例といえる。
 実験室で培養槽の様子を確認する。
実験室で培養槽の様子を確認する。
もちろん、量産化への道のりも容易なものではなかった。
「ラボスケールでは問題なく培養できていたのですが、スケールアップのために大きなタンクで培養すると、培養不良がおきました。原因はまったくわからず、原因を突き止めるのは大変でした。実機のタンクでテストするため、生産現場の方とも相談しながら、試行錯誤を繰り返しました。正直、製品化を諦めるという選択も頭に浮かびましたが、最終的に最適な培養条件を見出すことができ、製品化につなげることができました」と、小西は振り返る。
ナガセダイアグノスティックスと産総研チームの信頼関係は、いくつもの難関に立ち向かい、共に乗り越えることでより高まった。プロジェクトの後、産総研に移った酒瀬川は、企業と産総研それぞれの特徴を肌身で知る立場を存分に生かそうとしている。
「産総研の研究者たちの豊富な知見や広い観点での研究マネジメントの方法は、想像以上のものでした。一方で、産業界や顧客との距離の近さという点では、やはり企業のほうが勝っています。今後、産総研が社会実装をさらに進めるには、市場の顧客が求めるものをもっと知っていく必要があると思います」と語る。
「産総研には基盤技術をつくるという役割がありますが、技術を社会に実装していくうえでは企業との連携が不可欠です。今回は健康診断の検査試薬の原料という、一般の人もイメージしやすい成果が出せました。今後も、この成功をモデルにした共同研究を進めていきたいと思っています」と、安武も語る。
ナガセダイアグノスティックスとしては、酵素生産において、従来の方法に加えてスマートセルという技術を他社に先駆けて手中にできたことが成果の一つであった。スマートセルを用いた製造は、生産量が向上してロットサイズが大きくなることで品質がより均一化され、CO2削減や環境負荷の低減にもつながると期待されている。産総研から知的財産権に関する助言もあり、村松は「生産技術の選択肢が増え、企業としての独自性が高まった」と述べている。
今後はバイオものづくりの幅をさらに広げるため、新たなプロジェクトが両者間で始動する可能性もある。さらなる成果実現への期待が高まっている。
 スマートセルを用いたCE製造工程のスケールアップの様子。
スマートセルを用いたCE製造工程のスケールアップの様子。
*1:旭化成ファーマ株式会社診断薬事業部等は事業再編により、2025年7月1日付けで長瀬産業株式会社のグループ会社として新規に設立されたナガセダイアグノスティックス株式会社として営業を開始した。本文中の役職等は基本的に2025年7月時点のものを示す。詳細は2025年5月1日付けナガセダイアグノスティックス株式会社プレスリリースを参照。(産総研外のウェブサイトに移動します。)[参照元へ戻る]
*2: 国立研究開発法人新エネルギー・産業技術総合開発機構(NEDO)「植物等の生物を用いた高機能品生産技術の開発」(2016年度~2018年度委託事業、2019年度~2020年度助成事業)[参照元へ戻る]
*3: プロモーターとは、DNAからタンパク質をつくる際に重要な働きをする遺伝子配列のこと。今回成果につながったのは、常に働いている構成型のプロモーターである。[参照元へ戻る]
ナガセダイアグノスティックス株式会社
診断薬事業部
開発研究部 探索研究課
主幹研究員
村松 周治
Muramatsu Shuji
バイオものづくり研究センター
統括研究主幹
酒瀬川 信一
Sakasegawa Shin-ichi
ナガセダイアグノスティックス株式会社
診断薬事業部
酵素製品部 営業課
マネージャー
小西 健司
Konishi Kenji
バイオものづくり研究センター
応用機能分子デザイン研究チーム
主任研究員
安武 義晃
Yasutake Yoshiaki
ナガセダイアグノスティックス株式会社
診断薬事業部
開発研究部 技術開発課
研究員
村田 里美
Murata Satomi
ナガセダイアグノスティックス株式会社
産総研
生命工学領域
バイオものづくり研究センター