独立行政法人 産業技術総合研究所【理事長 野間口 有】(以下「産総研」という)エネルギー技術研究部門【研究部門長 長谷川 裕夫】エネルギー界面技術研究グループ 周 豪慎 研究グループ長、独立行政法人 日本学術振興会(JSPS) 王 永剛 外国人特別研究員は、大容量で、リサイクルが容易な「リチウム-銅二次電池」を開発した。
リチウムイオン電池は携帯電話やノートPCなどに広く使われているが、最近では自動車用として大容量化を目指した研究開発が行われている。また、将来的なリチウム資源の制約に対応できる低コストで再生可能なリチウム電池の開発が求められている。
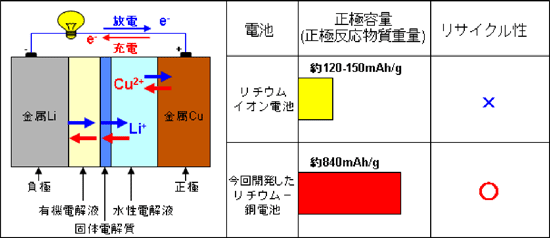
今回開発したリチウム-銅二次電池では、金属リチウムからなる負極側に有機電解液を、金属銅からなる正極側に水性電解液を用い、両電解液を固体電解質の壁で仕切り、両電解液の混合を防いだ。固体電解質の壁はリチウムイオン(Li+)だけを通すので、銅イオン(Cu2+)は有機電解液に到達せず、電池内の反応は支障なく進んだ。この電池の正極側の放電容量密度は、843mAh/g(正極で反応した銅重量あたり)であり、従来のリチウムイオン電池の5倍以上と大容量である。また、100回の充放電試験後も、放電容量の低下は微小であった。さらに、従来のリチウムイオン電池は、電極の構造が複雑なため寿命の尽きた同電池のリサイクルは極めて困難であるが、今回開発の電池は、電極には単純な金属リチウムと銅だけを用いているので、低コストで生産でき、簡単なプロセスでリサイクル可能である。
本研究成果は、2009年8月26~27日(現地時間)に米国サンノゼで開催されるIBM社主催のScalable Energy Storage大会で発表される。
 |
|
左図:新型「リチウム-銅二次電池」の構成、右図:従来技術との性能比較
単位は正極に使う活物質の重量あたりの放電容量(mAh/g)
|
リチウムイオン電池は携帯電話やノートPCなどに広く使われ、電気自動車用途に向けて大容量化の研究開発が行われている。しかし、現在のリチウムイオン電池には、正極にコバルトやマンガンなどを用いるという資源的な問題があるほか、高温焼結と微細な構造の制御など、複雑かつ高コストな製造プロセスが必要である。また、数百から数千回の充放電後、寿命の尽きた電池をリサイクルする際の問題として、活物質と導電助剤、カーボン、集電極との分離が難しい点が挙げられる。このような問題を克服するため、リサイクルが容易で、低コスト、大容量のリチウム電池の開発が望まれている。
産総研エネルギー技術研究部門では、次世代「リチウムイオン電池」の研究開発の過程で、電極材料をナノ構造化することで電池の大出力化が期待できることを示した(2005年1月18日、2007年11月19日、2008年8月27日 産総研プレス発表)。また、電気自動車用として、さらに大幅なエネルギー密度の向上が可能となる「リチウム-空気電池」(2009年2月24日 産総研プレス発表)の研究開発も行ってきた。これらのリチウム電池研究開発のポテンシャルを活かして、容易にリサイクルできる大容量リチウム電池の研究開発を行っている。
なお、今回の研究の一部は、独立行政法人 日本学術振興会(JSPS)の科学研究費補助金により行った。
今回、金属リチウムからなる負極側に有機電解液、金属銅からなる正極側に水性電解液を用い、両電解液を固体電解質の分離壁で仕切る構造の二次電池を開発した。分離壁により両電解液は混合しない。また、固体電解質壁はリチウムイオン(Li+)だけを通し、銅イオン(Cu2+)は有機電解液に到達しないため、安定した電池反応(充放電反応)が実現した。
充電時の電極における反応は次のようになる。
1)負極での反応:Li
+ + e
- → Li
リチウムイオン(Li+)は正極側の水性電解液から固体電解質壁を通り抜けて負極表面に達し、そこで配線から電子e-が供給されて、金属リチウム(Li)の析出反応(めっき)が起こる。
2)正極での反応:Cu → Cu
2+ + 2e
-
金属銅が銅イオン(Cu2+)として水性電解液に溶解し、電子e-は配線に供給される。
放電時の電極反応は次のようになる。
1)負極での反応:Li → Li
+ + e
-
金属リチウムがリチウムイオンとして有機電解液に溶解し、電子e-は配線に供給される。溶解したリチウムイオンは固体電解質を通り抜けて正極側の水性電解液に移動する。
2)正極での反応:Cu
2+ + 2e
- → Cu
銅イオンは正極側の水性電解液から正極表面に達し、そこで配線から電子e-が供給され、金属銅の析出反応(めっき)が起こる。
 |
|
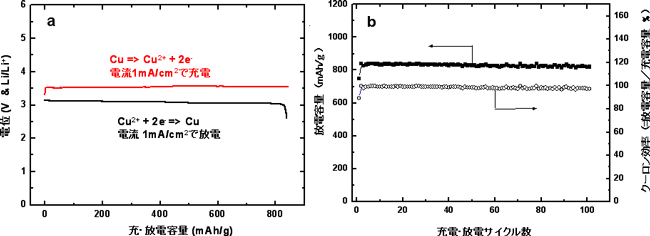
図1 今回開発した電池の充電・放電曲線(左)と、充電・放電特性(右)
|
今回開発したリチウム-銅二次電池の、正極の放電容量密度は約843 mAh/gとなり、充電容量密度も約843 mAh/g(正極で反応した銅重量グラムあたり)となった。この放電容量は、従来型のリチウムイオン電池の正極容量(120~150 mAh/g:文献値)に比べると大幅に増加している。右図に示すように100回の充電・放電後も、放電容量の低下は極めて微小であった。
このリチウム-銅二次電池は、電極に単純な金属のみを使っている。充電と放電の過程では、金属と金属イオンとの変化、すなわち金属の溶解・析出反応(めっき)を利用しているため、使用後も活物質は金属のままであり、電極金属のリサイクル(活物質の回収と再生)が容易である。また、水性電解液と有機電解液は固体電解質の分離壁で仕切られており、両者を個別に再生できる。これらにより、従来電池と比較してリサイクルが極めて容易であり、リサイクルコストを極めて低く抑えることができる。
この電池の充電・放電反応は、金属表面での金属イオンの溶解と、金属表面が金属イオンによって「めっき」される反応だけであり、化合物形成のような複雑な過程がないため、理論的には大きな電流密度での使用も可能である。ただし、現段階では固体電解質の分離壁のリチウムイオンの伝導率が十分ではなく、今後、出力密度を改良していく必要がある。
今回開発したリチウム-銅二次電池は、放電容量は従来のリチウムイオン電池の5倍以上と大きいが、電気自動車などのハイパワー用途には、さらに出力密度を向上させることが必要である。このためには、分離膜として用いた固体電解質のリチウムイオン伝導率を高めることが必要となる。産総研ではリチウム-銅二次電池の高出力化を目指して、今後さらに研究開発を進める予定である。