国立研究開発法人 産業技術総合研究所(以下「産総研」という)エネルギープロセス研究部門 エネルギー変換プロセスグループ 倉本 浩司 研究グループ長、笹山 知嶺 研究員、高坂 文彦 主任研究員らはデルフト工科大学 浦川 篤 教授と共同で、発電所や産業分野から排出されるガスあるいは大気中の低濃度CO2(400ppm(0.04%)~20%程度)から、液体燃料や化学品製造の原料として汎用性の高い合成ガスを直接製造する技術を開発した。
この技術は、CO2を選択的に吸収する機能と、吸収したCO2を水素(H2)との反応によって一酸化炭素(CO)に還元する機能を併せ持つ二元機能触媒を利用するものであり、低濃度CO2の分離・濃縮工程なしで、再エネ由来水素との反応により、一酸化炭素と水素の混合ガスである合成ガスを直接製造することが可能である。CO2を一酸化炭素に還元する反応では、一般的に白金やロジウムなどの遷移金属を用いた触媒が必要と考えられ、高活性な金属種の探索が進められてきた。しかし、本技術では遷移金属を使用せず、ナトリウムなどのアルカリおよびアルカリ土類金属を主成分とする単純な組成の二元機能触媒を用いてCO2を還元する。従来のCO2を原料とする合成ガス製造では、生成ガスに未反応のCO2が混入するが、本技術では生成ガス中にCO2はほとんど含まれない。さらに、水素の供給流量などを変化させることで、合成ガスの組成として重要なH2/CO比の制御も期待できる。したがって、この技術を既存の合成ガス利用プロセスと組み合わせることにより、下記のフロー図に示すように排ガスや大気中のCO2を出発原料として液体燃料や化学品を製造することが可能となり、本プロセスの実現によって、カーボンニュートラル社会の構築に大きく貢献できる。
なお、この技術の詳細は、2022年5月13日に国際誌 Journal of CO2 Utilizationにオンライン掲載される。
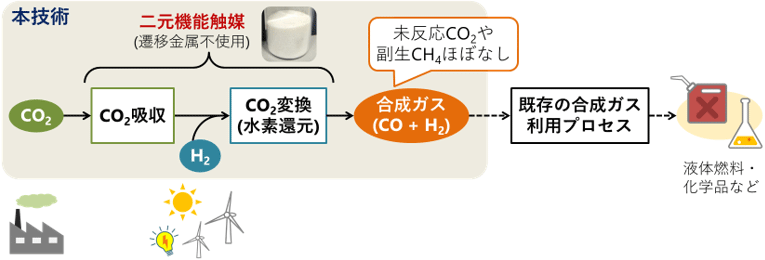
本技術を核としたCO2有効利用フロー
わが国では、2050年までに温室効果ガスの排出を全体としてゼロとする「2050年カーボンニュートラル」が政府目標として宣言され、CO2排出量の大幅削減が求められている。そのためには、既存プロセスの効率化によって大気中へのCO2排出を抑制するだけでなく、CO2を資源と捉え、これを燃料や化学品に変換して有効利用するCCUプロセスの開発も重要である。その中核となるのが、CO2から一酸化炭素と水素の混合ガスである合成ガスを製造する技術である。合成ガスを液体燃料や化学品に変換するプロセスは既に確立されており、排ガスや大気中のCO2から合成ガスを効率的に製造することができれば、大気中に廃棄されていたCO2を原料とした液体燃料や化学品の製造(フロー図)が実現する。
CO2から合成ガスを製造するには、水素との反応によってCO2を一酸化炭素に還元する逆シフト反応(CO2 + H2 → CO + H2O)を利用する。この逆シフト反応を効率的に進行させるためには、従来、活性の高い白金やロジウム、ニッケルあるいは銅などの遷移金属が触媒成分として必要であると考えられてきた。また、発電所や工場からの排ガスや大気中に含まれるCO2の濃度は400ppm(0.04%)~20%程度であるため、逆シフト反応操作の前にCO2を化学吸収プロセスで分離回収し、100%近い濃度にまで濃縮する必要があった。しかし、この分離や濃縮に要するエネルギー消費やコストが高いことから、低濃度のCO2から分離や濃縮工程を経ることなく、直接合成ガスを製造できる技術が必要とされている。そのための一方策として近年、CO2の吸収・変換機能を併せ持つ二元機能触媒を用いた新たな技術が注目されている。
産総研では、CCUのための触媒や反応プロセス開発に取り組み、低濃度CO2を都市ガス原料であるメタン(CH4)に変換する技術を開発した(2021年2月25日 産総研プレス発表)。この技術は、CO2を吸収するためのアルカリ金属(ナトリウム)と、CO2をメタンに変換するための遷移金属(ニッケル)を主成分とした二元機能触媒を用いるもので、CO₂分離・濃縮のための化学吸収プロセスを必要とせずに低濃度のCO2から高濃度のメタンを直接製造することが可能である。しかし、メタンの反応性は低いので、これをさらに変換して付加価値の高い化学品を製造するには多大なエネルギーが必要となる。すなわち、CO2由来のグリーンメタンは、天然ガス代替燃料が主な用途になると考えられる。本研究では、メタンよりも容易に高付加価値化できる合成ガスの製造に着目した。
既往のCO2変換に関する研究は、優れた触媒の開発のため、活性の高い遷移金属の種類や配合比を探索することが重要であった。しかし、我々は、遷移金属を使用せず、ナトリウムなどのアルカリおよびアルカリ土類金属を主成分とした二元機能触媒が、CO2の吸収と吸収したCO2を一酸化炭素に還元する機能を併せ持つことを世界に先駆けて見いだした。そして、このような遷移金属を使わない点で画期的な二元機能触媒を用いて、大気濃度のCO2から分離や濃縮工程を経ることなく、液体燃料や化学品製造に適した組成の合成ガスを製造することを目指した。
排ガスや大気中に存在するCO2を触媒自身が選択的に吸収し、吸収したCO2から合成ガスを製造する二元機能触媒として、ナトリウム種をアルミナ担体(γ-Al2O3)に分散させたNa/Al2O3を調製した。ナトリウム種の前駆体には炭酸ナトリウム(Na2CO3)を用いた。この二元機能触媒は遷移金属を用いていないことが特長であり、触媒の原料や製造工程の簡素化とそれによる低コスト化が期待できる。この触媒60 gを固定層反応器に充填し、500 ℃でCO2の吸収と変換挙動を調べる実験を行った。まず、CO2を窒素(N2)で希釈して大気中のCO2を模擬した濃度400ppm(0.04%)の混合ガスを反応器に供給した。触媒上に存在するナトリウム種の炭酸化反応(Na2O + CO2 → Na2CO3など)の進行によりCO2が吸収されるため、実験開始から約4時間の間CO2はほとんど流出しなかった(図1-①)。その後、触媒が吸収しきれなくなったCO2が次第に流出した。次に、窒素ガスを供給して反応器内に残存するCO2を押し出した後、水素ガスの供給を開始した。水素を供給し始めると、一酸化炭素が速やかに放出された(図1-②)。これは、触媒に吸収されたCO2と水素により逆シフト反応が進行したためと考えられる。一酸化炭素濃度の瞬間値は20%を超えており、CO2供給濃度の500倍以上に達した。
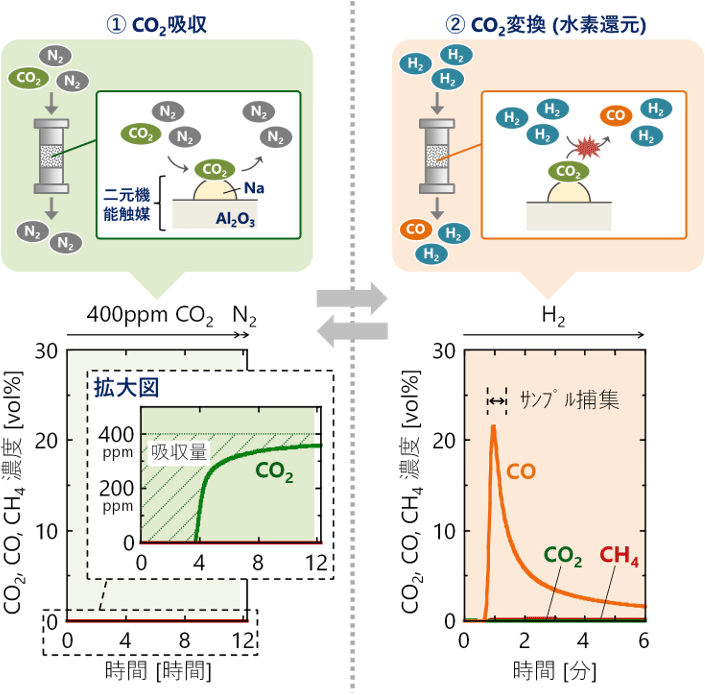
図1 Na/Al2O3二元機能触媒を用いたCO2吸収・変換実験
上記の吸収CO2の一酸化炭素への変換反応を利用して、合成ガスの製造の可能性を検討した。合成ガスは一酸化炭素と水素の混合ガスであり、液体燃料や化学品の製造原料となる。合成ガスの利用には、一酸化炭素の濃度だけでなく、未反応の水素とのモル比(H2/CO比)の制御が重要である。例えば、液体燃料を製造するためのフィッシャー・トロプシュ合成や、化学品製造の原料となるメタノール合成のためには、合成ガスのH2/CO比は2~3の範囲に制御する必要がある。そこで、前述の図1-②の一酸化炭素ピーク周辺の出口ガスをサンプルとして捕集し、組成を分析した。その結果を図2に示す。一酸化炭素と水素の濃度はそれぞれ14.5%、48.1%であり、H2/CO比は3.3であった。また、副生するメタンや未反応のまま流出するCO2はごくわずかであった。捕集した出口ガスにはその他のガスが約3割含まれていたが、これは主にCO2の希釈や押し出しに用いた窒素ガスであり、目的外の成分が生成した訳ではない。以上の結果は、一酸化炭素の生成量と未反応の水素量を適切に制御することにより、望ましいH2/CO比の合成ガスを製造できる可能性を示している。今後の研究で反応器の形式や水素流量などの反応条件を工夫することで、目的のH2/CO比の合成ガスを連続的に製造できると期待できる。
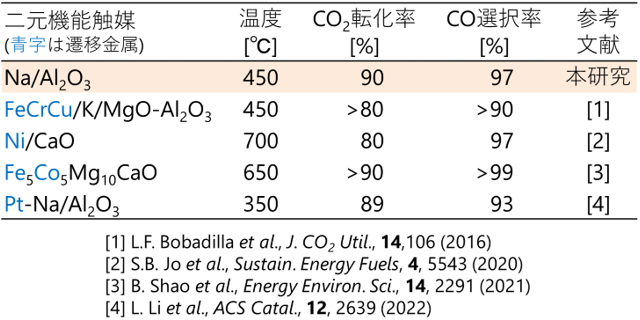
反応効率などをより詳細に検討するため、1 gのNa/Al2O3触媒を固定層反応器に充填した小スケールの実験装置を用いて、同様にCO2吸収・変換実験を行った。その際、反応温度は450 ℃、CO2吸収でのCO2の供給濃度は産業分野から排出されるガスを想定して5%とした。実験結果を基に、触媒に吸収されたCO2がどれだけ他の物質に変換されたかを表すCO2転化率と、生成物のうちどれだけ一酸化炭素が得られたかを表すCO選択率を算出した。それらの値を、二元機能触媒を用いてCO2吸収と一酸化炭素への変換を行った既往の研究と比較して表1に示す。逆シフト反応によってCO2を一酸化炭素に効率的に変換するためには、一般的に活性の高い遷移金属を用いた触媒が不可欠とされており、反応温度が高い条件が望ましい。本研究では、遷移金属を使用しない極めて単純な組成の二元機能触媒を用い、既往の研究の中でも比較的低温の450 ℃という反応条件で、90%以上の高いCO2転化率とCO選択率を達成した。
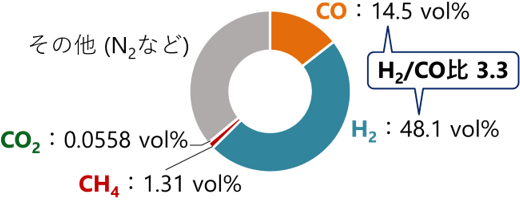
図2 捕集した出口ガスの組成
表1 二元機能触媒を用いてCO2吸収・変換実験を行った既往の研究との比較
この二元機能触媒の耐久性を確認するため、前述の1 gスケールの実験装置を用いて、450 ℃でCO2吸収(濃度5%)と一酸化炭素への変換を交互に繰り返し行った。図3に、触媒質量当たりのCO2吸収量と一酸化炭素生成量の推移を示す。各サイクルのCO2吸収量と一酸化炭素生成量はおおむね一致しており、触媒に吸収されたCO2が蓄積せずにほぼ全て一酸化炭素として放出されたことを意味する。実験を50サイクル繰り返したところ、CO2吸収量および一酸化炭素生成量はどちらも安定しており、大きな減少は観察されなかった。したがって、Na/Al2O3二元機能触媒は耐久性が高く、さらに長い期間繰り返し利用できる可能性が高い。
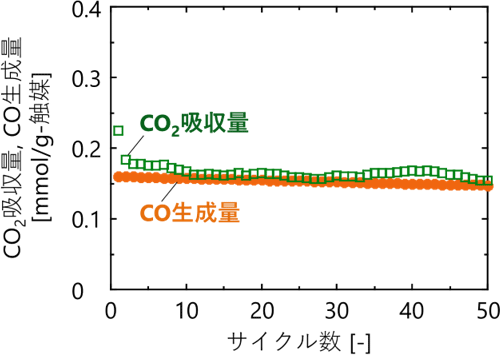
図3 繰り返し実験でのCO2吸収量と一酸化炭素生成量の推移
以上より、遷移金属を用いず、ナトリウム種のみをアルミナ担体上に分散させた極めて単純な組成の二元機能触媒が、大気濃度のCO2から合成ガスを直接製造できるポテンシャルを持つことを明らかにした。
今後は詳細な反応機構解析を行い、その結果に基づいて二元機能触媒のCO2吸収量や一酸化炭素生成速度のさらなる向上を目指す。また、反応条件の制御によって目的のH2/CO比の合成ガスを定常的に製造できる実用的な連続反応プロセスの開発にも取り組む。
掲載誌:Journal of CO2 Utilization
論文タイトル:Integrated CO2 capture and selective conversion to syngas using transition-metal-free Na/Al2O3 dual-function material
著者:Tomone Sasayama, Fumihiko Kosaka*, Yanyong Liu, Toshiaki Yamaguchi, Shih-Yuan Chen, Takehisa Mochizuki, Atsushi Urakawa, and Koji Kuramoto