独立行政法人 産業技術総合研究所【理事長 吉川 弘之】(以下「産総研」という)生物機能工学研究部門【研究部門長 巌倉 正寛】機能性核酸研究グループ 富田 耕造 研究グループ長、董 雪松 産総研特別研究員、沼田 倫征 研究員、渡邉 和則 産総研特別研究員、竹下 大二郎 専門技術者(財団法人 日本産業技術振興協会)らは、鋳型非依存性RNA合成酵素(以下「CCA付加酵素」という)が誤った配列を合成するのを回避するユニークな分子機構を明らかにした。
細胞内でタンパク質が合成される際、必要なアミノ酸を運んでくるtRNA(転移RNA)という70-90ヌクレオチドのRNA1本鎖がある。このtRNA鎖の大部分はDNAを鋳型として合成されるが、tRNA鎖末端にある3つのヌクレオチド配列CCAだけはCCA付加酵素という特別なRNA合成酵素によって合成されている。この合成は3ステップですすむが、合成の最後(Aの付加)の段階になって初めて、それまで合成された配列(CC)を酵素が確認するというユニークな機構であることがわかった。
本研究により、RNA合成酵素のデザイン開発が加速され、医療技術やバイオテクノロジーへの応用が期待される。本成果は、2008年7月23日に、EMBO ジャーナルに掲載される予定。
 |
|
|
tRNA合成の最後の段階で初めて、それまでに合成された配列CCをチェックする機構
|
細胞内における遺伝情報の流れはDNA→mRNA→タンパク質であり、DNA鎖を鋳型としてmRNA鎖が合成される。またDNAの複製時には、DNA鎖を鋳型として新たなDNA鎖が合成される。これらの合成は正確になされなければならないが、誤ったヌクレオチドを取り込む確率はゼロではない。誤って合成されてしまったときには、誤ったヌクレオチドを取り除く校正(プルーフリーディング:proofreading)機能や、相補的でないヌクレオチド対を含む二重鎖を見つけて優先的に切断してしまうシステムがあり、最終的に誤った配列をもったDNA鎖が生体内で合成されてしまう確率は10-7~10-8程度にまで低くなっている。
一方、生体内には鋳型を用いることなく、定まった配列を合成する鋳型非依存的RNA合成酵素が存在するが、これらは、校正機能を有していない。そのため、鋳型非依存的なRNA合成酵素が、誤った配列を合成する確率を低くする分子機構は謎であった。近年、生体内における鋳型非依存的RNA合成酵素による鋳型非依存的なRNA付加が、機能を持たないRNAの分解に積極的に関与していることが報告されてきている。すなわち、新たなRNAの品質を管理する役割をもっているといえる。したがって、鋳型非依存的RNA合成酵素の詳細な反応機構の研究は、新たな遺伝子発現制御解明において重要な役割を担っている。
産総研では、鋳型を用いないで定まった塩基配列を持つRNA鎖を合成する酵素、すなわち鋳型非依存的なRNA合成酵素の研究をしている。
これまでに、tRNAの3’末端に普遍的に存在するCCA配列を鋳型なしで合成する酵素、CCA付加酵素について一連のX線結晶構造解析によって30年間謎であった反応過程を解明(2006年10月16日 プレス発表)した。
今回、誤った配列のtRNAが合成される確率を低くする分子基盤を明らかにするため、末端に誤ったヌクレオチドを導入したRNAとこの酵素との複合体11種のX線結晶構造解析、さらにその構造を基にした生化学的解析を行った。
本研究は、独立行政法人 科学技術振興機構戦略的創造研究推進事業個人型研究(さきがけタイプ)「RNAと生体機能」【研究総括:野本 明男】からの研究補助金によっておこなわれた。また、X線結晶回折実験は大学共同利用機関法人 高エネルギー加速器研究機構 物質構造科学研究所の放射光科学研究施設のビームラインBL-5A、AR-NW12、NW-17を使用した。
tRNAは細胞内でタンパク質が合成される際に、アミノ酸の運び屋として働いているRNA1本鎖であり、常時30種から40種のtRNAが細胞内で働いている。全てのtRNAの3'末端にはCCAという配列が存在し、その末端塩基Aにアミノ酸が結合して、必要とされる場所にアミノ酸が運ばれる。tRNA本体の大部分の70-90塩基のRNA鎖はDNAを鋳型として合成されるが、末端のCCA配列だけはCCA付加酵素とよばれる鋳型非依存性RNA合成酵素によって合成される。
このCCA配列はtRNAがタンパク質合成で機能するために必須な配列であり、CCA配列以外の配列を持つtRNAはタンパク質合成できない。CCA付加酵素は、鋳型を用いることなく定まった配列を合成することができる鋳型非依存的なRNA合成酵素である。CCA付加酵素には間違ったヌクレオチドをRNAの末端へ付加したときに、それを削除する校正機能を有さないことが知られている。これまで、CCA付加酵素が誤った配列を合成してしまったときに、どのようにして機能を持たないtRNA産物が極力生産されないようにするのかわかっていなかった。
今回、CCA付加酵素と3’末端に変異を導入したRNAとの複合体(9種類)さらにCCA付加酵素と変異RNAと付加されるヌクレオチドの複合体(2種類)の計11種類の複合体のX線結晶構造解析を行った。また、3’末端に変異を導入したRNAへのヌクレオチド(CTPあるいはATP)の付加反応の生化学的解析を行った。2006年に我々はCCA付加酵素によるC付加およびA付加反応における酵素、RNAの動的な反応分子基盤を明らかにしている。C付加反応では、酵素は開いた構造から閉じた構造へ変化し、それに伴ってRNAの末端部分が反転し、酵素とRNAのダイナミックな動きで反応が進行する。一方、A付加反応では、酵素は最初から閉じた構造をとっており、かつRNAの末端は反転しており、酵素とRNAのダイナミックな動きは伴わない(図1)。
|
|
|
図1 CCA付加酵素によるC付加反応(左)とA付加反応(右)での酵素、RNAの動き
|
今回の変異RNAを用いた生化学的解析およびX線結晶構造解析から、以下のことが明らかになった。
生化学的解析から
|
1) |
CCA付加酵素は1番目にC以外の間違ったヌクレオチドを付加しても、酵素はその誤りを認識せず、2番目のC付加反応が進行してしまう。しかし最後のA付加反応は著しく抑えられている。 |
|
2) |
RNAの末端の配列がCC、CUあるいはUCのときのみ最後のA付加反応が進行するが、それ以外の組み合わせではA付加反応は進行しない。 |
また、X線結晶構造解析(図2、3)から
|
3) |
2番目のC付加反応は、1番目にC以外の間違ったヌクレオチドが付加されていても、酵素は開いた構造をとっており、CTPが酵素に結合して閉じた構造に変化し、それに伴ってRNAの末端部分が反転して反応が進行する。(図2) |
|
4) |
最後のA付加反応のステップにおいて、閉じた酵素とRNAの3’末端部分で1番目と2番目に正しいヌクレオチドが付加されているかどうかを確認している。1番目あるいは2番目の位置にCC以外の間違ったヌクレオチドが付加されていると、酵素とRNAの3’末端部分は開いた構造をとり、付加されるATPとRNAの3’末端で立体障害が生じる。(図3、4) |
|
5) |
末端がCUあるいはUCの場合には、RNAの3’末端部分が、半分反転した構造をとっており、CCの場合のようにATPが結合できるため、末端が反転して、Aが付加される。また、末端がCAの場合には、反応が進行するために必要なRNAの末端ヌクレオチド(A)の反転ができないため、末端がCAのRNAへはAが付加されない。 |
|
|
|
図2 CCA付加酵素と末端に変異を導入したRNAとの構造(2番目のC付加反応)
|
|
|
|
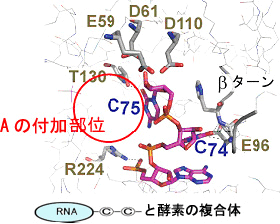
図3 CCA付加酵素と末端に変異を導入したRNAとの構造(最後のA付加反応)
|
以上の生化学的、構造学的解析から最後のA付加反応が進行するための条件は
|
1) |
最初のヌクレオチドの塩基部分C74と酵素がワトソン-クリック様水素結合を形成すること。 |
|
2) |
2番目のヌクレオチドの大きさ及び塩基部分C75と酵素との水素結合を形成すること。 |
この2つがが協同的に働くことである。
|
|
|
図4 tRNA末端合成の正しい配列維持のための末端配列モニター機構
|
このことは合成反応の最終のA付加の段階になって、初めて、それまでに合成された2個の配列CCを酵素が確認するという仕組みである。この研究で明らかになったCCA付加酵素によるtRNA合成の正しい配列維持の機構は、通常の鋳型依存的なDNA・RNA合成酵素には見られない新しい分子機構である。合成時における正しいヌクレオチドの選択以外に、末端配列をモニターすることによって、末端に誤ったヌクレオチドの入ったtRNAが合成する可能性を低くしている。この分子機構は、RNAとタンパク質が協同で機能を発現していることを示す例でもある。
今後、他の種類の鋳型非依存性RNA合成酵素についても同様な解析をすすめ、RNAとタンパク質が協同で機能発現するからくりの解明をめざす。