国立研究開発法人 産業技術総合研究所【理事長 中鉢 良治】(以下「産総研」という)創薬分子プロファイリング研究センター【研究センター長 夏目 徹】構造モダリティ研究チーム 竹内 恒 研究チーム長とハーバード大学 医学部 ダナファーバーがん研究所のHari Arthanari博士らは、従来とは異なり炭素とフッ素の原子核間相互作用を活用してNMRの観測感度などを向上させ、従来と比べて一桁大きい分子量10万を超える大きなタンパク質の芳香族アミノ酸残基側鎖のNMR観測に成功した。
バイオ医薬の開発や品質評価を行うために、その高次構造を、溶液状態のまま解析する技術の確立が求められている。NMR法は生体高分子の高次構造を溶液中でそのまま解析でき、近年、バイオ医薬の開発や品質評価のための分析技術としての応用が期待されている。しかし、分子量が大きくなるほど感度が低下する課題があり、特にバイオ医薬の機能部位に多く存在し、標的との結合を担う芳香族アミノ酸残基の側鎖については、分子量3万程度がNMR観測の限界で、抗体などの分子量10万を超えるバイオ医薬では、NMR観測が困難だった。
今回開発したNMR手法では、分子量18万の芳香族アミノ酸側鎖にフッ素を導入してのNMR観測や、抗体(分子量15万)など高分子量バイオ医薬のありのままでの高次構造分析・評価を実現できる。また、創薬の研究・開発においても、阻害剤・賦活剤の開発や高機能化などさまざまな可能性を拓くものである。なお、この技術の詳細は、2019年3月11日(英国時間)にイギリスの科学誌Nature Methods誌に掲載される。
 |
|
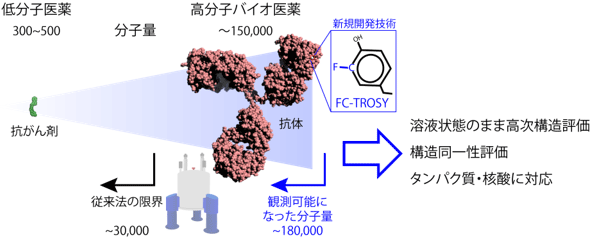
高分子バイオ医薬の分子量とNMR観測が可能な範囲 |
バイオ医薬は、現代医療には不可欠であり、低分子医薬が効かない標的に対して、高い特異性で薬効を示す。バイオ医薬の多くは有効成分がタンパク質などの生体高分子であるため、分子サイズが大きく、バイオ医薬の一種である抗体医薬では分子量が15万にも達する。一方、バイオ医薬の薬効や副作用は、高次構造を反映して大きく変わる。例えば、長期保存などによりバイオ医薬が劣化し、高次構造が変化すると、薬効が失われたり、副作用が増強したりする。
このように高次構造が極めて重要なバイオ医薬の品質評価や開発では、ありのままの高次構造を解析する技術が求められている。しかし、これまでの高次構造解析手法では、バイオ医薬に対して何かしらの手を加える必要があり、それにより、高次構造が変化する可能性を排除できなかった。
また、溶液中の酵素の活性部位や標的分子の薬剤結合部位の高次構造を明らかにすることは、酵素の活性を強化したり、薬剤との結合解析を通じて阻害剤や賦活剤の開発を行ったりする際にも、不可欠な情報を与える。そのため、創薬の研究・開発のためにも、溶液中でありのままの高次構造を解析する手法の開発が求められていた。
産総研では、NMR法を用いた創薬支援基盤技術の開発と社会実装に取り組んでおり、低分子医薬だけでなく、バイオ医薬など新たな医薬品を視野に入れた研究開発を進めている。特に、生体高分子の高次構造を溶液中でそのまま解析できるNMR法の開発と応用に力を入れており、今回、ハーバード大学医学部ダナファーバーがん研究所と、抗体など分子量15万を超えるタンパク質の、芳香族アミノ酸側鎖のNMR観測を可能にする新たな手法の開発を進めた。
NMR法は、溶液中の生体高分子のありのままの高次構造を原子レベルで解析できる優れた特性を持ち、バイオ医薬の高次構造評価への応用が期待される。しかし、標的との相互作用部位に多く存在する芳香族アミノ酸残基の側鎖については、高分子量になると感度低下が特に著しく、従来法では分子量3万程度が観測の限界であった。そのため、抗体など分子量の大きなバイオ医薬の機能を担う核心的部分について、NMR法で高次構造を分析・評価することは難しかった。
今回、これまで着目されてこなかったフッ素核(F)と炭素核(C)の原子核間の干渉を利用して、芳香族アミノ酸残基側鎖のNMRシグナルの感度を大幅に向上させる「FC-TROSY法」を開発した。なお、測定する芳香族側鎖には、本来フッ素が含まれないので、あらかじめ側鎖にフッ素を導入した試料を測定する。これまでTROSY法は、水素核(H)と窒素核(N)か水素核と炭素核との干渉を利用して、高分子量のタンパク質をNMR観測する方法として知られてきた。芳香族アミノ酸残基側鎖に対しては水素核と炭素核の干渉を利用するHC-TROSY法が用いられるが、高分子量領域では、感度が不十分で芳香族側鎖が観測できなかった。一方、フッ素核と炭素核の干渉を利用するFC-TROSY法では、芳香族側鎖を、HC-TROSY法より一桁高い感度で測定できた。
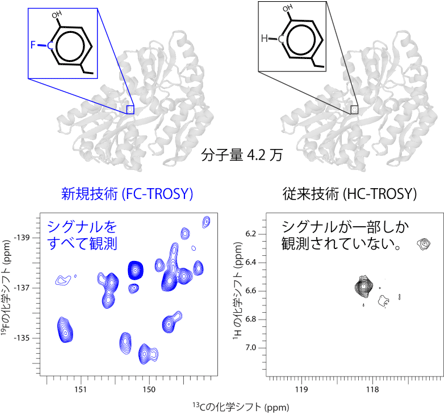
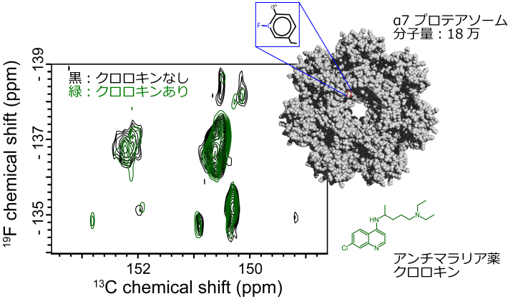
分子量が約4.2万のタンパク質の芳香族アミノ酸残基のうちチロシン残基にフッ素を導入し、今回開発したFC-TROSY法と従来のHC-TROSY法を用いてNMRで観測した。その結果、HC-TROSY法では、理論的に予想される数よりも少ない、3個のシグナルしか観測されなかったが(図1右)、FC-TROSY法では強いシグナルが、チロシン残基の数だけすべて観測され、感度が格段に向上したことが確認できた(図1左)。また、分子量が一桁大きいタンパク質(分子量18万)でも、FC-TROSY法によりNMRシグナルが観測できた。さらに、このタンパク質と阻害剤を結合させるとNMRシグナルが変化することも観測できた(図2)。
 |
|
図1 今回開発したFC-TROSY法(左)とHC-TROSY法(右)で観測した芳香族アミノ酸のシグナル |
 |
|
図2 FC-TROSY法(図1左)により分子量18万のタンパク質を観測 |
フッ素核は、これまでもタンパク質に導入され、NMR観測に利用されてきた実績があり、市販の分光器で測定できる。また、フッ素核の導入によるタンパク質の高次構造の変化は無視できると考えられている。FC-TROSY法を活用すると、抗体など高分子量のバイオ医薬のありのままの高次構造を評価できると期待される。加えて新しい手法では、高分子量酵素の活性部位や、膜タンパク質を含むレセプターのリガンド結合部位の高次構造解析にも広く応用が可能である。さらに、新たな医薬として着目されている核酸医薬でも、同様の感度増大が期待できるため、高分子量の核酸医薬への適用も期待される。
今後は抗体医薬など実際の高分子量バイオ医薬や創薬標的タンパク質を用いて、それらの高次構造を評価する技術を開発し、社会実装していく。また、NMR法を用いた創薬支援基盤技術を発展させて、低分子、バイオ医薬、中分子など多様な医薬に対応できる創薬基盤技術プラットフォームを構築する予定である。