国立研究開発法人 産業技術総合研究所【理事長 中鉢 良治】(以下「産総研」という)先進コーティング技術研究センター【研究センター長 明渡 純】エネルギー応用材料研究チーム 間宮 幹人 主任研究員、秋本 順二 研究チーム長は、導電性基板上に蒸着でナノメートルスケールの一酸化ケイ素(SiO)薄膜を形成し、その上に導電助剤を積層させた構造のリチウムイオン2次電池用電極(負極)を開発した。この積層構造を有する電極の充放電特性は、容量が現在主流である黒鉛負極(372 mAh/g)の約5倍に相当し、一酸化ケイ素の理論容量2007 mAh/gとほぼ一致した。また、開発した電極は充放電を200サイクル以上繰り返しても容量は維持され、高容量で長寿命な特性を持つことが明らかとなった。今回開発した電極により、負極のエネルギー密度が向上し、リチウムイオン2次電池の高容量化や小型化が促進されると期待される。
なお、この技術の詳細は、2018年11月27~29日に大阪府立国際会議場(大阪市)で開催される第59回電池討論会で発表される。
 |
|
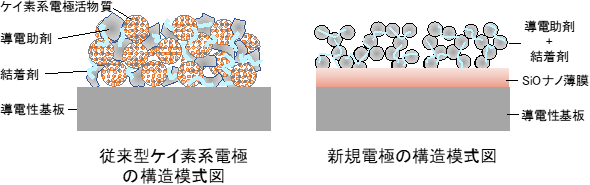
従来型電極と今回開発した電極の構造の模式図 |
スマートフォンや電気自動車などリチウムイオン2次電池の市場は急速に拡大しており、市場調査会社の予測によると2021年には2015年の約2倍の4兆円規模に成長するとされている。市場拡大に伴い電池の高性能化や安全性の向上に向けた開発が盛んに行われている。負極としては従来の黒鉛より数倍から十数倍の理論容量を持ち供給の安定性に優れたケイ素系負極が次世代負極の最有力とされている。中でも一酸化ケイ素は、汎用の黒鉛負極(372 mAh/g)に比べて、理論容量が2007 mAh/gにも達するため期待されている。現行の塗工法で作製した一酸化ケイ素電極でも、1200 mAh/g程度の容量を示すが、容量のサイクル劣化の問題が残り、一酸化ケイ素単体では実用化されていない。一方、一酸化ケイ素と黒鉛の混合物を用いた電極が開発され、黒鉛電極の2倍を超える800 mAh/g程度の容量の製品が市場へ出始めているが、一酸化ケイ素材料本来の性能を十分引き出すには至っていない。
産総研では、次世代の2次電池の開発を材料化学の見地から進めてきており、正極、負極、固体電解質と電池全般の部材用の新規材料開発に取り組んできた。一酸化ケイ素は蒸気圧が高く、高温減圧条件下で容易に気化するため、蒸着で一酸化ケイ素薄膜を基板上に成膜できる点が利点である。しかし、一酸化ケイ素自体は導電性が極めて低いため、一酸化ケイ素の蒸着薄膜を直接電極として用いる発想はなかった。今回、電極材料として用いるため、蒸着条件や導電性を付与するためのプロセスについて検討を進めてきた。
リチウムイオン2次電池は正極と負極の間をリチウムイオンが移動することで充放電できる(図1)。電池の高容量化には一酸化ケイ素を負極活物質に用いることが有望であるが、ケイ素は充放電に伴うリチウムイオンの取り込みと放出で300 %以上の体積変化が生じるため、活物質、導電助剤、結着剤からなる電極構造が維持できなくなり劣化してしまう。粒径を300-500 nm以下まで微細化すれば劣化の抑制効果が見られるため、一酸化ケイ素の薄膜を作製し、劣化の改善を目指した。
集電体であるステンレス上に一酸化ケイ素を蒸着した。導電性を付与するため、導電助剤としてカーボンブラックに結着剤を加え分散させた混合液を、蒸着した一酸化ケイ素膜の上から塗布・乾燥させて導電助剤層を作製した。この電極は一酸化ケイ素薄膜上に導電助剤層を積層させた構造となる。
作製した電極の断面電子顕微鏡写真を図2に示す。蒸着で得られた一酸化ケイ素は、ステンレス基板上に膜厚80 nm程度の薄膜を形成していた。導電助剤のカーボンブラックは50 nm 程度の粒子が結着して鎖状となり、その端部はこの一酸化ケイ素薄膜に接していた。一酸化ケイ素の膜厚は、充放電による劣化の抑制効果があるとされる300 nmよりも薄く、微細化された組織であることが確認できた。
この電極を負極とし、正極としてリチウム(Li)を用いた電池の充放電容量のサイクルごとの変化を図3に示す。また、比較のために以前からある粒径10 µmの一酸化ケイ素粉末で作製した電極と、現行の材料である黒鉛を用いた電極を用いた電池の特性を合わせて示す。粉末を用いた電極ではサイクルに伴う容量劣化が顕著であり、一方、黒鉛電極ではサイクル劣化は見られないが、容量は372 mAh/gと小さかった。これに対して、今回の電極は、1サイクル目から大きな容量が得られると共に、その後の充放電でも安定した容量を保ち、200サイクルを経ても2000 mAh/g以上の容量を示した。2サイクルから200サイクル目まで容量維持率は97.8 %を示し、200サイクルでのクーロン効率は99.4 %と、充放電におけるリチウムの取り込みと放出が可逆的に行われていることがわかる。今回得られた2000 mAh/gを超える容量は一酸化ケイ素の理論容量2007 mAh/gとほぼ一致し、電極を構成する一酸化ケイ素のほぼ全てを電池の活物質として利用できていることを示している。
今回開発した電極は、導電性の低い一酸化ケイ素の膜厚をナノメートルサイズまで薄くし、その上に導電助剤層を積層して導電性を確保するという新しい発想で作製されたもので、膜厚の薄さによりサイクル劣化の問題が克服されると同時に、効率的に電極活物質を利用できる。
 |
|
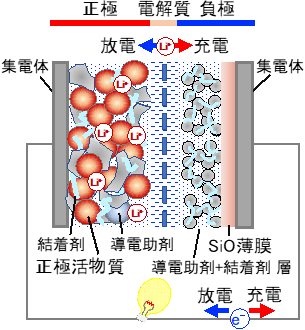
図1 今回開発の負極を用いるリチウムイオン2次電池の概略図
外部から電気エネルギーを与え正極活物質からリチウムイオンを放出させ負極活物質に取り込ませた(充電)後、負極活物質からリチウムイオンを放出させ正極活物質に取り込ませる(放電)化学反応から電気エネルギーを取り出す仕組みを組んだものをリチウムイオン電池と言う。さらにこのサイクルを繰り返し利用できるものをリチウムイオン2次電池と呼ぶ。 |
 |
|
図2 新規積層電極の断面電子顕微鏡写真
ステンレス基板にナノメートルスケールの一酸化ケイ素膜が蒸着し、導電助剤であるカーボンブラック粒子が結着剤で連結して一酸化ケイ素薄膜に接している。 |
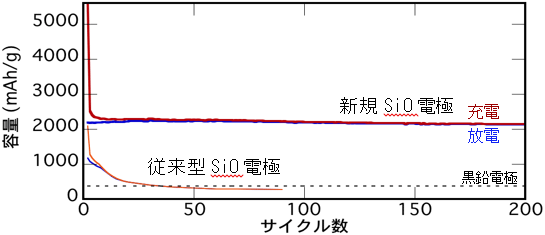 |
図3 今回開発した電極と従来型電極を用いて作製した電池の充放電サイクル特性
2032型コインセルを作製し対極 リチウム、電流値 0.1 C、温度25 ˚C、 電圧範囲0-2.0 Vで評価。
従来型電極は粒径10 µmの粉末SiOを電極に使用した時の結果。 |
今回開発した電極は、図3に示すように、初回充電時に大きな容量を必要とする。これは充放電に関与しないリチウムケイ素酸化物(Li4SiO4)が生成する反応のためで、このまま電池として組むと正極のリチウムが消費され性能が低下してしまう。今後は、この問題を避けるためにあらかじめリチウムと反応させるプレドープという処置を施した電極を準備し、既存の正極と組み合わせた電池を作製して実用化に向けた性能実証試験を行う。また、蒸着法やそれ以外の方法を用いてスケールアップの検討も併せて行う。