国立研究開発法人 産業技術総合研究所【理事長 中鉢 良治】(以下「産総研」という)バイオメディカル研究部門【研究部門長 近江谷 克裕】分子細胞育種研究グループ 芝上 基成 上級主任研究員は、株式会社 アルチザンラボ【代表取締役 柴田 みなみ】(以下「アルチザンラボ」という)、株式会社 神鋼環境ソリューション【社長 粕谷 強】(以下「神鋼環境ソリューション」という)と共同で、ミドリムシ(EOD-1株)由来の多糖類(パラミロン)から水溶性高分子を作製し、メタボリックシンドロームに関連する指標を改善する作用を示すことを確認した。
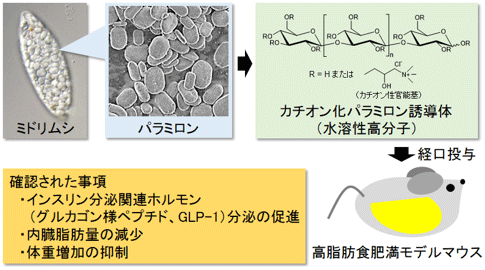
パラミロンは水に溶けない多糖類であるが、カチオン性官能基を導入したカチオン化パラミロン誘導体は水溶性となる。今回、高脂肪食肥満モデルマウスにこの誘導体を与えたところ、マウスの内臓脂肪量が減少し、体重増加の抑制作用が確認された。また、インスリン分泌に関与するため糖尿病治療薬開発の重要なターゲットとなっているホルモン(グルカゴン様ペプチド-1(GLP-1))が、この誘導体を投与しなかった対照群に比べて3倍多く分泌されることが確認された。さらに、インスリン抵抗性が改善された可能性があると考えられた。
なお、この技術の詳細は、平成30年5月24~26日に東京国際フォーラム(東京都千代田区)他で開催される第61回日本糖尿病学会年次学術集会で発表される。
 |
|
ミドリムシ由来の物質、カチオン化パラミロン誘導体によるメタボリックシンドローム改善効果の可能性 |
近年、日常生活が健康上の問題で制限されない期間、つまり健康寿命を延ばすためのさまざまな取り組みが注目を集めている。その取り組みの大きな障害の一つがメタボリックシンドロームと、それにより発症リスクが高まる疾病、特に糖尿病である。糖尿病はさまざまな合併症を引き起こすが、糖尿病の三大合併症の一つとされている糖尿病腎症に至ると、血液透析などを行っても、生命予後は不良とされている。
これまで糖尿病に至る前のメタボリックシンドロームの治療では、食事制限や運動が行われてきたが、その効果は個人差が大きいため、効率よく内臓脂肪を抑制する薬剤が求められている。現在、食欲抑制剤としてサノレックス一種だけが国内で使用できるが、うつ病などの副作用が問題とされている。また近年では、胆汁酸吸着レジンが、脂質異常症に対する効果に加えて、糖尿病に対する効果が注目を集めているが、使用により膨満感や便秘、まれに腸管穿孔や腸閉塞に至った症例が報告されている。
GLP-1は、インスリン分泌を促すホルモンのひとつであることから、糖尿病治療薬開発の重要なターゲットであるが、生体内では数分以内に壊れてしまうためその作用を長続きさせるための薬剤の開発が続けられている。また、2型糖尿病患者ではGLP-1分泌量が少ないことから、その分泌を刺激する薬剤の開発も求められていた。
パラミロンはミドリムシの細胞内に大量に蓄積され(乾燥重量で最大80 %程度)、容易に抽出・精製できる。また、純度はほぼ100 %であり、高分子鎖長がほぼ揃っている。産総研は、これまでパラミロンに着目し、これを出発原料とするさまざまな素材の研究開発を行ってきた(2013年1月9日 産総研プレス発表)。一方アルチザンラボは、医療に関する知見・技術を保有し、神鋼環境ソリューションはミドリムシの大量培養技術を保有している。そこで三者は糖尿病治療薬の開発を念頭に、糖尿病を含むさまざまなメタボリックシンドロームの改善に有効と考えられる胆汁酸吸着機能を持つカチオン化パラミロン誘導体の開発と、その薬効の評価に取り組んだ。
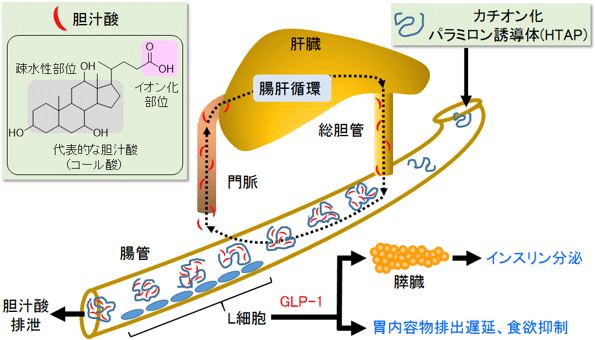
胆汁酸は、腸管内で脂肪とともにミセルと呼ばれる小胞体を形成し、小腸上皮細胞から吸収されるが、吸収された胆汁酸の大半は再利用される(これを腸肝循環という)。従来の多くの胆汁酸吸着剤に共通する作用メカニズムは、腸管内で胆汁酸を吸着して排泄することで胆汁酸の腸肝循環が妨げられ、肝臓内でコレステロールから胆汁酸への合成が進行し、結果としてコレステロールの血中濃度が低下することになると考えられている。そこで、この作用メカニズムに則り、カチオン化パラミロン誘導体の分子設計を行った。
今回合成したカチオン化パラミロン誘導体(2-ヒドロキシ-3-トリメチルアンモニオプロピルパラミロン、HTAP)は、パラミロンの構成単位であるブドウ糖ひとつあたりのカチオン性官能基の置換数(degree of substitution (DS))が約0.8~1と高く、また多くのカチオン間の反発のため腸管内では一本鎖の状態となる。したがって、導入したカチオン性官能基の多くが胆汁酸のアニオン性部位と結合できると期待される。加えて、カチオン化後もパラミロン本来のらせん形成能は保持されうるため、らせん構造内部に胆汁酸の疎水性部位を収容する疎水性の空間が構築されることも期待される。
 |
|
カチオン化パラミロン誘導体(HTAP)によるGLP-1分泌促進 |
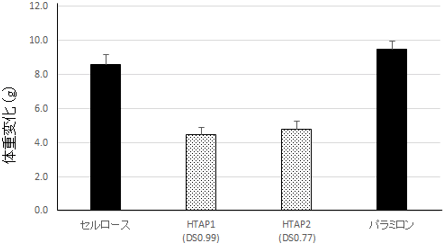
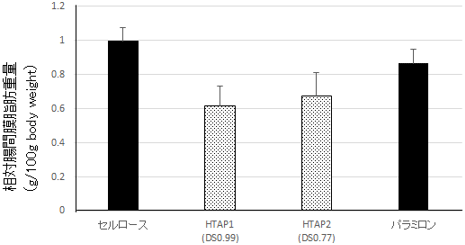
HTAPを2 wt%含む高脂肪食をマウス(初期体重は約28 g)に5週間に渡って与え、その体重、内臓脂肪量、各種血漿パラメーターなどを測定したところ、同量のセルロースを与えた対照群と比較して、体重増加は50 %程度に抑制され(図1)、内臓脂肪量(腸間膜脂肪重量)は33~38 %減少した(図2)。これらは統計上有意な差である。また、対照群とほぼ同レベルの血糖値を維持するためのインスリン分泌量が低下したことから、インスリン抵抗性が改善された可能性が考えられる。
 |
|
図1 セルロース、カチオン化パラミロン誘導体(HTAP)、パラミロンを含む高脂肪食を与えたマウスの5週間後の体重変化量 |
 |
|
図2 高脂肪食を与えたマウスの体重100 gあたりの相対腸間膜脂肪重量 |
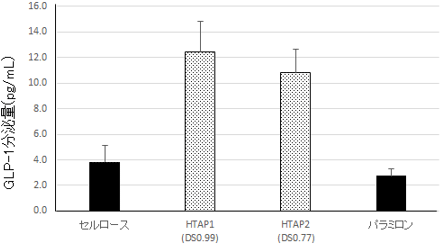
腸管L細胞から分泌される消化管ホルモン(GLP-1)は「痩せるホルモン」と呼ばれているが、今回、HTAPを与えることでGLP-1の分泌が対照群に比べて3倍程度増加したことが分かった(図3)。GLP-1にはインスリン分泌を促進する効果があるが、促進作用は血糖値に依存するため低血糖などの副作用を引き起こすリスクは少ないとされる。加えて、胃内容物の排出を遅らせる効果や食欲抑制効果もある。これらの一連の効果は糖尿病治療に望ましいためGLP-1は近年の糖尿病治療薬開発の重要なターゲットとなっている。今回の研究開発で確認されたHTAPによるGLP-1分泌促進の詳細な作用メカニズムは現段階では不明であるが、試験管実験では胆汁酸の親水性・疎水性の性質や分子構造に応じてカチオン化パラミロン誘導体への吸着効率が異なることから、誘導体を投与したことで、腸管内での胆汁酸の組成や分布に変化が生じたのではないかと考えられる。その結果、腸管下部のL細胞の表面に存在する胆汁酸受容体のより高い活性化が引き起こされ、GLP-1の分泌が促進されたと考えられる。
 |
|
図3 高脂肪食を与えたマウスのGLP-1分泌量 |
今後はパラミロン誘導体によるGLP-1分泌促進の作用メカニズムの解明とパラミロンやその誘導体の構造の最適化を念頭に、大学などの研究機関や製薬企業を含めた新たな研究開発体制の構築に取り組む。