国立研究開発法人 産業技術総合研究所【理事長 中鉢 良治】(以下「産総研」という)生物プロセス研究部門【研究部門長 田村 具博】兼 産総研・東大先端オペランド計測技術オープンイノベーションラボラトリ【ラボ長 雨宮 慶幸】津田 栄 上級主任研究員、同部門 近藤 英昌 主任研究員、西宮 佳志 主任研究員らと、国立研究開発法人 量子科学技術研究開発機構【理事長 平野 俊夫】(以下「量研」という)量子ビーム科学研究部門【部門長 茅野 政道】安達 基泰 上席研究員らは共同で、氷結晶に似た水分子のネットワークが不凍タンパク質(AFP)の表面に形成されていることを発見した。また、この水分子のネットワークが正四面体型構造の水分子クラスタを含むときに、氷に結びつく力が最も強くなることを明らかにした。魚類やキノコから得られるAFPは産業・医学応用が進んでいる凍結制御物質で、水が凍る寸前に生まれる小さな氷に結合して凍結を抑制すると考えられてきた。今回の発見によって、AFPが瞬時に氷に結合して氷の成長を抑制できる理由が初めて説明された。今後、分子表面に氷結晶に似た水分子ネットワークが形成される物質を人工的に作製できれば、細胞や組織を0 ℃より少し低い温度で凍結保存できる新たな省エネ技術につながると期待される。
なお、この研究の詳細は、学術誌Proceedings of the National Academy of Sciences USA(米国科学アカデミー紀要)に近日中にオンライン掲載される。
 |
|
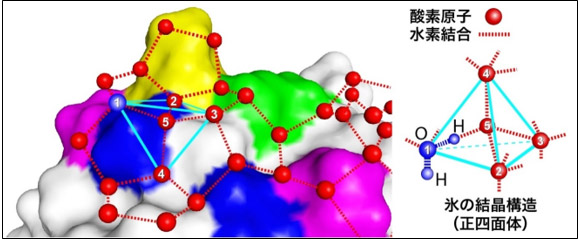
AFP表面に形成された氷結晶に似た水分子ネットワーク(正四面体を形成した5個の水分子を含む) |
氷は、水が凍結する瞬間に発生する無数の小さな氷が時間と供に成長と融合を繰り返してできたものであり、0 ℃以下では際限なく大きくなる性質をもつ。氷が大きくなり続ける現象が凍結保存中の食品、医療品、細胞、組織などの内部で起こるため、それらの凍結品質や生命力が損なわれることが問題になっている。AFPは、0 ℃より少し低い温度域で氷の表面に結合し、それらの成長と融合を強く抑制できるが、もしもAFPをお手本に人工凍結制御物質を作製し、個々の氷を極小サイズに留めることができれば、僅かな冷熱のエネルギーで含水物中に氷の塊を作らせない新たな冷凍技術ができると期待されている。また、そのような物質は、氷を極めて細い針状に変形させる技術などにも活用できると考えられている。しかし、AFPが瞬時に氷に結合できる理由や、AFPの構造構築原理に対する理解は十分ではなく、AFPの構造と機能の分子レベルでの解明が強く望まれていた。
産総研では産業や医学の分野でAFPを高度利用するための研究を進めてきた。魚類を原材料とするAFP大量精製技術や高気孔率セラミックスを製造するためのAFPゲル化凍結技術などを開発する一方、菌類AFPの分子構造解明やAFPの細胞生存率改善効果の発見、連結して氷の成長を止めるAFPの発見などの成果もある。また、2016年には共同研究先企業によって魚類の天然AFPが製品化され、その活用方法が現在検討されている。より高度な技術開発を目指し、近年はタンパク質結晶作製技術に強みを持つ量研と共同でAFPの表面にある水分子に注目した研究を行っていた。
なお、本研究は日本学術振興会科学研究費助成事業(15K13760)による支援を受けて行った。
今回用いたⅢ型AFP(アミノ酸残基数65、分子量約7,000)は、産総研が2005年にゲンゲ科魚類(図1(A))から発見したもので、このAFPの野生型は(1)氷結晶のプリズム面などに結合する平らな分子表面を備え、(2)その中央付近にあるアミノ酸残基であるアラニン残基(A20)が氷結晶面に対する結合力に深く関係している(図1(B))。そこで、野生型のA20を、他のアミノ酸であるロイシン(L)、グリシン(G)、スレオニン(T)、バリン(V)、イソロイシン(I)に置換した変異体(A20L、A20G、A20T、A20V、A20I)を作製し(図1(C))、それぞれの氷に対する結合力を調べた所、図1(D)の様な差異を示した。このうちA20LとA20Iは側鎖のサイズが同一であるにも関わらず、氷結晶への結合力は著しく異なった(図1(C))。一方、γ位にメチル基をもつA20T、A20V、A20Iは何れも強い結合力を示した。それぞれの変異体のX線結晶構造解析から、氷との結合力が最も強いA20Iの分子表面に約50個の水分子からなる氷結晶に似た水分子のネットワークができていることが明らかになった。通常、水分子はタンパク質表面と水素結合を形成するが、疎水性のメチル基が導入されて水分子とタンパク質表面の水素結合形成が阻害されたために、水分子間での水素結合形成が強いられ、ネットワークが形成されたと考えられた。メチル基の導入によりA20T、A20V、A20I 上では5個の水分子が四面体を形成していたが、氷結晶と同じ完全な正四面体を形成していたのはA20Iだけであった(概要図)。この四面体構造の完全性と氷との結合力の間には正の相関があるため、氷結晶に似た水分子のネットワークは極めて限られた性質・形状のタンパク質表面にだけ形成されると結論付けた。
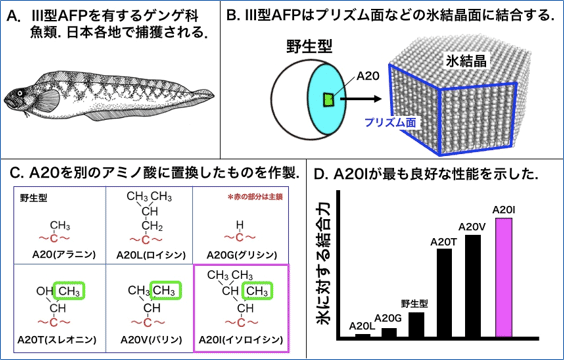 |
図1 ゲンゲ科魚類(A)から抽出される野生型Ⅲ型AFPの模式図(B)、野生型(A20)と今回作製した各種変異体(C)と、それらの氷との結合力(D)
Cの緑枠はγ位のメチル基を示す。 |
氷結晶の表面は厚さ約1.0-1.5 nmの乱れた成長界面になっている(図2)。今回の結果から、氷結晶に似た水分子ネットワークはこの成長界面と瞬時に混ざり合い、四面体型の水分子を氷結晶のプリズム面などの中に組み込んでAFPと氷結晶を強固に結びつけることにより、それ以上の氷の成長を止めると考えられた。また、この場合のエネルギー障壁は自由水が成長界面で氷結晶構造に変化する場合よりも低いと考えられた。氷結晶に似た水分子ネットワークを表面にもつ物質を創ることができれば、例えば僅かな冷熱エネルギーで氷の大きさを極めて小さなサイズに留めるなど、水の凍結現象を制御するさまざまな技術が開発できると期待される。
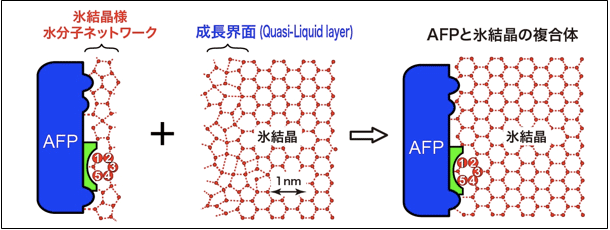 |
図2 AFP(A20I)の氷結晶結合モデル
氷結晶に似た水分子ネットワークが氷結晶の成長界面と混ざり合い、素早く強固なAFP-氷結晶の複合体ができると考えられた。
緑は導入したメチル基を表す。 |
今後は、AFP表面に氷結晶に似た水分子ネットワークが形成されるメカニズムをより詳細に解明し、AFPを手本にした人工凍結制御物質のデザインを検討する。また、凍結寸前に発生する無数の氷を極限まで小さくすることを目標に、そこに至るための方法論の確立を目指す。同時に、AFPに関する研究データを集積し、より高度なAFP技術の開発を目指す。