独立行政法人 産業技術総合研究所【理事長 中鉢 良治】(以下「産総研」という)集積マイクロシステム研究センター【研究センター長 前田 龍太郎】ライフインターフェース研究チーム 亀井 利浩 研究チーム長、住友 慶子 産総研特別研究員らは、面発光マイクロLED励起光源、およびアモルファスシリコン・フォトダイオードに光学干渉フィルターを一体的に集積した蛍光検出センサーから構成される超小型蛍光検出デバイスを開発した。面発光マイクロLEDからの光を非球面マイクロレンズにより、マイクロ流路幅以内に集光することに成功し、マイクロ流路への低散乱光照射を実現した。さらに、マイクロビーズを充填、固定化したマイクロ流体バイオチップにおいてイムノアッセイ(免疫定量法)が可能であることを示した。
この技術は、感染症の早期発見、在宅やベッドサイドでの健康モニタリング、個別化医療など、患者の傍らで、迅速な診断が求められるPoint-of-Care(POC)診断を実現するキーテクノロジーとして期待される。
なお、詳細は、2014年3月17日~20日に青山学院大学相模原キャンパス(神奈川県相模原市)で開催される第61回応用物理学会春季学術講演会で発表される。
 |
|
開発した超小型LED励起蛍光検出装置の外観(外寸40×40×20 ㎜) |
近年、その場で高速に診断できる利便性・簡易性からPOC診断が注目され、特に、糖尿病患者の血糖センサーは商業上も大きな成功を収め、POC診断市場全体としても急速に成長している。POC診断は、疾患の予防、健康増進に寄与し、患者の生活の質(Quality of Life)を維持しながら、医療費を削減できる在宅医療にも資する技術であり、今後、ますます発展すると期待される。POC診断は、医療従事者が実施する簡易診断および患者自身が在宅で実施する健康モニターなどの自己診断を含んでいるが、いずれの場合にも、可搬性、迅速性、簡便性が要求される。
微少量の流体を操作可能なマイクロ流体バイオチップ技術は、少量の試料での高速診断が可能であり、POC診断を実現するために理想的な特徴を備えている。また、マイクロ流体バイオチップを用いた、遺伝子、タンパク質、コレステロールなどの生体分子解析に基づく疾患の診断システムの開発が既に世界的に進められており、微少量の血液などの試料から疾患の状態を迅速・簡便に診断することが可能になっている。しかし、微少量の試料から分析するため、高感度な共焦点レーザー励起蛍光顕微鏡のような大型の装置が用いられており、マイクロ流体バイオチップは小型であるが、分析装置としては依然として大型である。産総研では、この大型の分析装置をPOC診断や着用可能(ウエアラブル)な健康モニタリングデバイスなどの“現場”に持ち込むため、バイオ分析の中心的な手法であり、多様な物質や用途に関する膨大な分析手法・手順を引き継ぐことができる蛍光検出分析装置の集積化・小型化に取り組んできた。
これまで、半導体微細加工技術により、アモルファスシリコン・フォトダイオード上に光学干渉フィルターを一体的に集積した蛍光検出センサー(図1)を開発してきており、外部励起光源を用いた実験において、PCRと組み合わせることでDNAを一分子レベルで検出できる検出限界を実現している。アモルファスシリコンはバイオ分析に使われる実用的な色素のほぼ全ての蛍光波長帯域で高効率に光を電流に変換させることができ、ノイズも少ないため、冷却せずに、蛍光を高感度に検出できる。しかし、本当の意味での集積型蛍光検出デバイスを実現するためには、励起光源の集積化・実装が必要であり、今回は、安価な面発光マイクロLEDを用いて、超小型蛍光検出装置を開発した。
なお、この研究開発は、総合科学技術会議により制度設計された最先端研究開発支援プログラム(平成21~25年度)により、独立行政法人 日本学術振興会を通して助成された研究課題「マイクロシステム融合研究開発(中心研究者:江刺 正喜 東北大学)」の一環として行われた。
 |
|
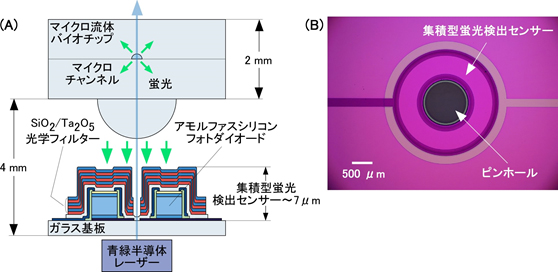
図1 (A)集積型蛍光検出センサーを用いたマイクロ流体バイオチップ分析システムの断面図、(B)センサー部の上部からの光学顕微鏡写真 |
今回開発した蛍光検出モジュールの大きな特徴は、励起光源と集積型蛍光検出センサーをマイクロ流体バイオチップに対して、同側に、かつ、同軸に配置している点にある。これは、図1に示されているように、可視光に対して透明であるガラス基板上に蛍光検出センサーを作製できること、および、その中央に励起光を導入するためのピンホールを形成したことにより可能になっている。
今回、励起光源として採用したLEDは、半導体レーザーの1000分の1程度の価格で、低コスト化に有利であるが、光の指向性が低く、集光することが難しい。集積型蛍光検出装置には、従来法(共焦点レーザー励起蛍光顕微鏡)で採用されているピンホールによる散乱光遮蔽機能がないため、励起光をマイクロ流体バイオチップ内のマイクロ流路幅以内に集光し、マイクロ流路側壁からの散乱を抑制することが特に重要である。散乱光は蛍光検出素子のバックグラウンド光電流となり、検出システムのノイズレベルは、このバックグラウンド光電流に重畳するノイズレベルで決まるため、検出システムのノイズレベルを下げるには、散乱光を抑制する他ない。
今回の研究においては、LED発光面の小型化および非球面マイクロレンズの採用により集光スポットを小さくしている。サイズが250×300 µmの面発光マイクロLEDからの光を非球面マイクロレンズにより短焦点(5 mm)で190×230 µmに集光することに成功し、バイオ分析に必要な光量を確保しながら、マイクロチャンネルへの低散乱光照射を実現した。さらに、小型のLEDを用いることにより、100 µm以下に集光することも可能である。
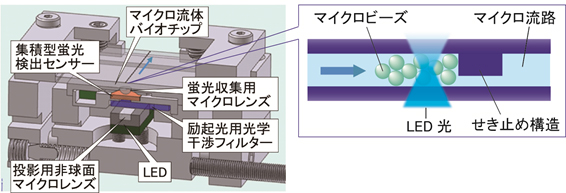
図2に今回開発した超小型LED励起蛍光検出装置(外寸40×40×20 ㎜;LED、蛍光収集用マイクロレンズ、集積型蛍光検出センサーなどの蛍光検出に関わる心臓部は15×5×6.4 ㎜)の詳細と流れ方向に沿ったマイクロ流路の断面構造を示す。面発光マイクロLEDから放出された光は非球面マイクロレンズにより集光され、励起光用光学干渉フィルターにより、特定の波長領域の光のみを選択的に取り出し、集積型蛍光検出センサーを介して、マイクロ流体バイオチップ内のマイクロ流路に照射される。マイクロ流路内の蛍光色素から放出される蛍光を蛍光収集用マイクロレンズにより収集し光学干渉フィルターにより選択的に蛍光成分のみを取り出し、アモルファスシリコン・フォトダイオードにより検出する。この蛍光検出装置を用いて、ポリスチレン製マイクロビーズ上に固定化された抗体を蛍光色素が結合したタンパク質(蛍光標識化タンパク質)により検出した。マイクロ流体バイオチップ内のマイクロ流路には、せき止め構造が形成されており、抗体が固定化されたポリスチレン製のマイクロビーズが充填、固定化されている。
 |
|
図2 LED励起蛍光検出装置の構造と流れ方向に沿ったマイクロ流路断面構造 |
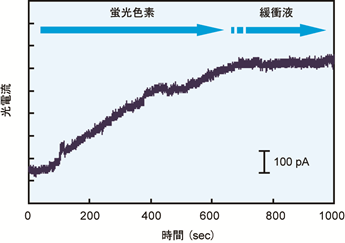
このような状態で、ビーズに固定化された抗体と反応する蛍光標識化タンパク質を導入し、続いて緩衝液を流し、その間の蛍光の時間変化を検出した(図3)。蛍光標識化タンパク質を流すと、時間経過とともにビーズ上の抗体との反応が進行して蛍光標識化タンパク質がビーズ上にトラップされ、蛍光強度が増加するが、緩衝液に切り替えると、反応が停止し、ビーズに固定化された蛍光標識化タンパク質からの蛍光が観察されるため、蛍光強度は飽和する。以上の結果は、この蛍光検出装置が臨床検査で重要なイムノアッセイを行えることを示している。
 |
|
図3 抗体との反応による蛍光強度の時間変化 |
今回開発した超小型LED励起蛍光検出装置は、これまで研究室にとどまっていたマイクロ流体バイオ分析技術を、POC診断、ウエアラブルな健康モニタリングデバイスなどの”現場”に持ち出すための新しい検出プラットホームであるといえる。
今後は、LEDが面発光源である特徴を生かして、LEDやマイクロレンズを量産性の高い実装技術を用いて組み立てる手法を確立するとともに、さらなる小型化と高感度化の両立を目指す。また、半導体レーザーのウエハーレベルパッケージング技術の開発も進めており、POC診断への早期の実用展開を図りたい。