独立行政法人 産業技術総合研究所【理事長 野間口 有】(以下「産総研」という)ゲノムファクトリー研究部門【研究部門長 鎌形 洋一】近江谷 克裕 主幹研究員、および、セルエンジニアリング研究部門【研究部門長 大串 始】セルダイナミクス研究グループ 呉 純 研究員は、国立大学法人 北海道大学【総長 佐伯 浩】大学院医学研究科 尾崎 倫孝 教授らと共同で、近赤外線発光タンパク質を創り出すことに成功し、これと医薬抗体とを結合させプローブ化することでがん細胞の位置を特定できる技術を開発した。
近赤外線発光タンパク質は、ウミホタルルシフェラーゼの糖鎖に近赤外線有機蛍光色素を導入することで得られた。この蛍光色素は生体内化学反応でエネルギーが移動することにより近赤外線を発光するが、近赤外線は生体透過性が高いので、生体内部の近赤外線発光を外部から観察できる。このような近赤外線発光タンパク質はこれまで存在しなかった。
また、近赤外線発光タンパク質と医薬抗体とを結合させて近赤外線発光プローブとすることで、マウス体内に移植した肝がん細胞をCCDカメラでモニターできることを明らかにした。今回開発した近赤外線発光プローブは化学反応で近赤外線を発光するので、外部から放射線や紫外線を当てる必要のないがん細胞評価法である。本プローブを用いることで医薬抗体の評価や病理ライブ診断など医療技術の革新が期待される。
なお、本研究成果の詳細は、9月7日(米国東部時間)、全米科学アカデミー紀要(Proceedings of the National Academy of Sciences USA, PNAS)に掲載される。
 |
|
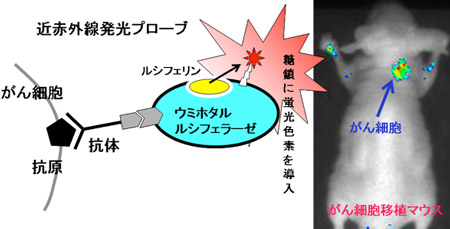
近赤外線発光プローブの概念図
|
国民の健康維持にはがん疾病対策が重要であり、微小ながん組織を徹底的に摘出する方法として、大規模施設を必要としない術中光診断法の開発が望まれている。一方、がんの新しい治療薬としてモノクローナル抗体、いわゆる医薬抗体が注目されている。医薬抗体はがん細胞に特異的な抗原を認識し、がん細胞を攻撃するものである。したがって、生体内における医薬抗体の動きを知ることは医薬抗体そのものの評価に大変重要である。また、抗体を利用してがん細胞を可視化し、微小ながん組織を特定できる可能性もある。
現在、生体内の抗体の動きをモニターする技術としては加速器によるポジトロンエミッショントモグラフィー(PET)法などが用いられているが、大型の機器、施設が必要で時間と経費がかかるため、医療現場での利用には制約が多い。GFP(緑色蛍光タンパク質)のような光プローブを利用する方法も考えられているが、GFPの蛍光は可視光線領域(波長範囲400-700 nm)で生体透過性が低く、その利用には限界がある。そこで注目を集めているのが、「生体の窓(特に波長範囲650-1000 nm)」と呼ばれる生体を透過する波長領域(波長範囲700-1400 nm)の近赤外線を利用することであるが、これまで実用レベルに達したものは少なく、開発が望まれていた。
産総研はウミホタル発光系に着目し、ウミホタルルシフェリンやウミホタルルシフェラーゼを大量生産する方法を研究開発してきた。また、北海道大学大学院医学研究科、株式会社リブテックと協力し、医薬抗体の候補の1つであるDLK-1抗体と発光タンパク質とを結合させた発光プローブの開発およびそれを利用した肝がん細胞の可視化に取り組んできた。
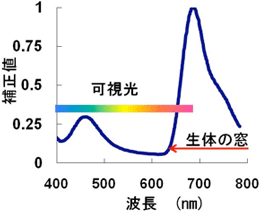
ウミホタルルシフェラーゼの糖鎖に近赤外線有機蛍光色素を導入し、人工的な生物発光共鳴エネルギー移動機構(BRET)によって生体内の化学反応のみで近赤外線を発する発光タンパク質(近赤外線発光タンパク質)を作製した。近赤外線は血液中のヘモグロビンに吸収されることが少ないので(図1)、生体内で発した近赤外線を外部のCCDカメラなどでモニターすることができる。従来の近赤外線を発する蛍光色素は、蛍光であるため外部光源を照射して発光エネルギーを与える必要があったが、今回作製した近赤外線発光タンパク質は生体内の化学反応により生じるエネルギーで近赤外線を発するので外部光源を必要としない。
 |
|
図1 血中における近赤外線発光タンパク質とウミホタルルシフェリンの発光スペクトル
|
近赤外線発光タンパク質を医薬抗体の候補の1つであるDLK-1抗体と結合させ、近赤外線発光プローブとした。このプローブをDLK-1抗原の発現した細胞の培地に入れ、120分程度培養後に細胞を洗浄し、培地にウミホタルルシフェリンを加えると、DLK-1抗原を発現する細胞だけが近赤外線を発することが観察された(図2)。これらのことから近赤外線発光プローブはDLK-1抗原を認識する能力と近赤外線を発する2つの機能を持っていることが確認できた。
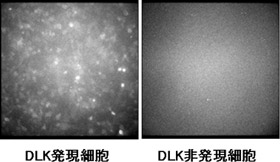
図2 近赤外線発光プローブによるDLK-1抗原発現細胞(左)と非発現細胞(右)の近赤外線映像
|
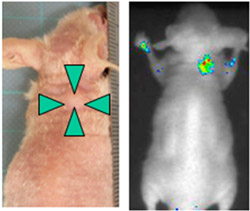
図3 肝がん細胞を移植されたマウスの外観(左)と近赤外線発光プローブによるDLK-1抗原発現がん細胞のライブ映像(右)
|
DLK-1抗原を発現する肝がん細胞をマウスに移植し、がん細胞が数mm程度の大きさに成長した段階で、近赤外線発光プローブを静脈より注入した。24時間後、同じく静脈よりウミホタルルシフェリンを注入してCCDカメラでマウスを撮影すると、がん細胞が移植された位置で近赤外線を発しているのが観察できた(図3)。なお、波長570 nm以下の光をカットするフィルターを用いて近赤外線領域を中心とする波長の発光を計測することにより、バックグラウンドの少ない鮮明な映像が得られた。
今回開発した技術のさまざまな抗体への適用を試み、抗体治療薬の開発、抗体を用いた外科手術における術中診断、ライブ病理映像や抗体による再生細胞の評価など、多方面の応用展開を目指したい。