独立行政法人 産業技術総合研究所【理事長 吉川 弘之】(以下「産総研」という)ゲノムファクトリー研究部門【研究部門長 鎌形 洋一】遺伝子発現工学研究グループ 田村 具博 研究グループ長は、旭化成ファーマ株式会社【代表取締役社長 稲田 勉】と共同で、免疫抑制剤として使用されているミゾリビン(MZR)の血中濃度測定に使用できる酵素(ミゾリビンリン酸化酵素)を見つけ、その効率的な製造方法を開発した。
ミゾリビンは、腎移植における拒否反応の抑制・ループス腎炎・慢性関節リウマチ等の治療などに広く用いられている低分子化合物(分子量259)である。しかし、ミゾリビンの効果と治療の安全性を確保するための至適量に関しては不明な点があり、個人ごとの最適な投与量を把握するためには、血中濃度を測定しながら投与量を調整することが必要であると指摘されている。
現在、ミゾリビンの血中濃度は、高速液体クロマトグラフィー(HPLC)によって測定できるが、手間と時間がかかる。今回開発した酵素を用いると、短時間で簡便な測定が可能となる。本技術の詳細は、2008年11月27日~30日に名古屋国際会議場で開催される「第55回日本臨床検査医学会学術集会」で発表される。
 |
|
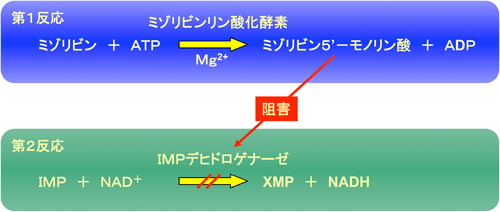
今回発見されたミゾリビンリン酸化酵素によるミゾリビン濃度の測定原理
|
|
NAD+:酸化型補酵素、 NADH:還元型補酵素
第2反応で生成するNADH濃度は、波長340ナノメートルの吸光度から容易に計測できるので、ミゾリビン濃度を算出できる。
|
ミゾリビン(MZR)は、腎移植における拒否反応の抑制・ループス腎炎・慢性関節リウマチ等の治療などに広く用いられている低分子化合物(分子量259)である。しかし、ミゾリビンの効果と安全性を確保するための至適量に関しては不明な点がある。ミゾリビンは同様の薬効を示す他の薬と比べて、白血球減少などの血液系障害が少ないものの、主として腎臓から排泄されるため、腎障害のある患者では排泄が遅延し、骨髄機能抑制等の重篤な副作用が起こることがある。そのため血中濃度測定による投与量の調整が必要であることが近年指摘されている。
現在、ミゾリビンの血中濃度は高速液体クロマトグラフィー(HPLC)による測定が可能である。しかし、HPLCによる測定は、(ⅰ)装置が限られた施設にしか配備されていない、(ⅱ)検体の前処理が必要である、(ⅲ)測定に時間を要すると共に多検体同時測定が出来ない、(ⅳ)血液の他の成分分析に比べて試料の必要量が多い(最低でも0.8ミリリットル)、などの問題点がある。そこで、より短時間で簡便な測定を実現するために、汎用自動分析機で測定可能なミゾリビンの血中濃度測定法の開発が望まれている。
産総研ゲノムファクトリー研究部門遺伝子発現工学研究グループでは、ロドコッカス属放線菌(Rhodococcus erythropolis)による化学物質やタンパク質の生産系を構築する研究を行ってきた。特に放線菌によるタンパク質の生産は、既存技術である大腸菌による生産が困難なタンパク質の生産を可能にする特徴がある。一方、旭化成ファーマ株式会社診断薬製品部では、診断薬用酵素の開発や、酵素を用いた診断薬の開発を行っている。そこで、産総研は旭化成ファーマ株式会社と共同で、ロドコッカス属放線菌を用いた診断薬用酵素製造技術の開発に取り組んできた。
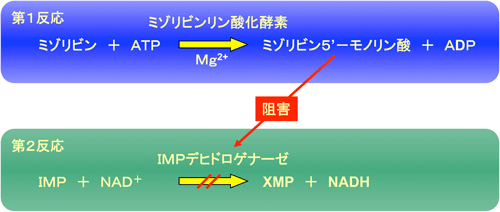
本技術によるミゾリビン濃度の測定原理は図1に示すような2つの反応からなる。
 |
|
図1 今回発見されたミゾリビンリン酸化酵素によるミゾリビン濃度の測定原理
|
|
NAD+:酸化型補酵素、 NADH:還元型補酵素
第2反応で生成するNADH濃度は、波長340ナノメートルの吸光度から容易に計測できるので、ミゾリビン濃度を算出できる。
|
第1反応では、ミゾリビンリン酸化酵素の働きで、ミゾリビンにリン酸が結合してミゾリビン5’-モノリン酸(MZR-P)になる。このMZR-PがIMPデヒドロゲナーゼという酵素の働きを阻害するので、第2反応ではその阻害の程度を測定することによってMZR-P濃度、すなわちミゾリビン濃度が算出される。IMPデヒドロゲナーゼという酵素は化合物IMP(イノシン一リン酸)を化合物XMP(キサントシン一リン酸)に変換する酵素であり、この時化合物NAD+(補酵素酸化型)が化合物NADH(補酵素還元型)になる。NADHの濃度は波長340ナノメートルの吸光度を測定することによって容易に測定できる。これによってIMPデヒドロゲナーゼの酵素活性の阻害の程度が算出され、MZR-P濃度からミゾリビン濃度が算出される。
第1ステップのミゾリビンをリン酸化する酵素は、ヒト生体内においてどの酵素がその役割を担っているか明らかになっていないので、ゲノム情報が登録されているデータベースの中から、予想される遺伝子を検索した。候補とした複数の遺伝子を組み換えタンパク質として大腸菌で発現させ、生産されたタンパク質がミゾリビンのリン酸化能力を有するかどうかの探索を行った。ところが、それらの酵素を大腸菌内で生産すると、生産された酵素により、細胞内の核酸やリン酸化された核酸の濃度バランスが崩されるために、大腸菌が死んでしまうことが多く、探索が進まなかった。
そこで、産総研のロドコッカス属放線菌(Rhodococcus erythropolis)を用いたところ、菌が死ぬことなく、探索が容易になった。さまざまな微生物由来の酵素遺伝子をこの放線菌で発現した。その結果、ミゾリビンをリン酸化する酵素遺伝子を発見した。さらに、その遺伝子を用いて放線菌でミゾリビンをリン酸化する酵素の効率的な製造方法も開発した。詳細に解析した結果、本酵素はバクテリアでは世界で初めて発見された核酸のリン酸化酵素(ヌクレオシドキナーゼ)であり、学術的にも価値の高い酵素である事が明らかになった。
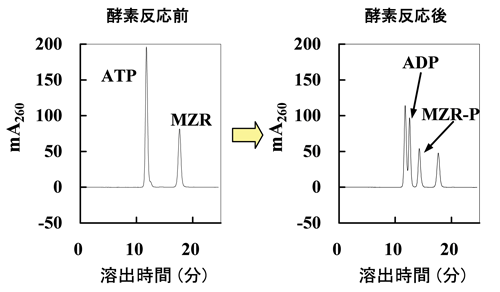
本酵素を用いて、ミゾリビン血中濃度測定の酵素法を開発した。第1反応でこの酵素によるリン酸化反応の様子をHPLCで解析した結果を図2に示す。反応途中なので未反応のATPとミゾリビンも残っているが、ATPがADPに変化され、ミゾリビンがMZR-Pに変換されていることが確認された。この第1反応は、5分間で完結する。
 |
|
図2 HPLCにより解析した本酵素によるミゾリビンのリン酸化反応(第1反応の確認)
|
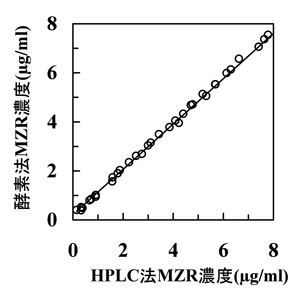
第1反応の反応液を第2反応の試験液(IMPとNAD+とIMPデヒドロゲナーゼを含む)に加えて第2反応を行い、波長340ナノメートルの吸光度の測定を行った。吸光度からIMPデヒドロゲナーゼの酵素活性の阻害の程度が算出され、MZR-P濃度、ミゾリビン濃度の算出を行った。その結果、図3のようにHPLCを用いた濃度測定結果と一致することから、正確に血中に存在するミゾリビン濃度の測定ができることが確認された。
 |
|
図3 酵素法ミゾリビン(MZR)血中濃度測定結果とHPLC法との比較
|
現在、ミゾリビン血中濃度測定は、検体の前処理時間を除いたHPLC測定だけでも18分必要で1時間に3.3検体しか測定できない。このミゾリビン血中濃度測定酵素法を利用すれば汎用の生化学自動分析機による多検体同時測定が可能で、1時間に600検体測定できるようになる(汎用生化学用自動分析機、日立7080形自動分析機を使用した場合)。
この研究成果をもとに、産総研はミゾリビン(MZR)をリン酸化するヌクレオシドキナーゼの機能解析をさらに進め、旭化成ファーマ株式会社はミゾリビン血中濃度測定試薬を開発する予定である。