独立行政法人 産業技術総合研究所【理事長 吉川 弘之】(以下「産総研」という)エレクトロニクス研究部門【部門長 和田 敏美】機能集積システム研究グループ【グループ長 金丸 正剛】亀井 利浩 主任研究員は、アモルファスシリコン・フォトダイオード上に光学干渉フィルターを集積化したマイクロ蛍光検出センサ(検出限界:フルオレセイン7nM(ナノモラー:1リットル中あたり10億分の1モルの濃度)を開発した。
さらに、健康工学研究センター【センター長 国分 友邦】生体ナノ計測チーム【グループ長 石川 満】と共同で、マイクロ流体電気泳動チップと組み合わせた手のひらサイズのコンパクトなデバイス(図1)で、高速(2分程度)、高感度(DNA検出限界:約250pg(ピコグラム:ピコは、1兆分の1)/µL)、高分解能(理論段数:約70000)でDNA断片の分離・検出に成功した。
本技術は、家庭用CD/DVDドライブ程度の大きさで、DNA、RNA、たんぱく質、糖鎖等の高速分析用装置への発展も可能であり、手術や救急車の緊急医療や災害現場等、医療処置が必要なその場(Point-of-Care)での高速バイオ分析に道を開くものである。
|
|
|
図1.マイクロ蛍光検出センサを実装したポータブルな高速DNA分析装置。 |
最近のヒトゲノム解読や疾病に関する分子的理解の進歩に伴い、特定の疾病に関する疾病マーカー分子や、個々人の遺伝情報の差違による疾病のかかり易さ、薬の副作用の違いなど、数多くのことが判明してきている。
しかしながら、それらの成果を直接、手術中や救急車での搬送中など緊急医療や災害現場での治療に用いるためには、疾病マーカーをその場で高速に検出・同定し、患者の遺伝的体質を迅速に判定することが必要になる。また、通常の医療現場でも患者の遺伝情報に基づく診断・投薬・治療(
テーラーメイド医療)が求められていることなど、現場ですぐ使える高速でかつ高精度なポータブルバイオ分析装置へのニーズが高まっている。
現場ですぐ使える高速でかつ高精度なポータブルバイオ分析装置へのニーズに対応するために、患者に負担をかけない極少量のサンプルで、高速で、かつ高精度で分析を行えるマイクロ流体バイオチップが開発されてきた。しかしながら、検出すべきターゲット物質が極僅かなため、手のひらに乗るような小さなマイクロ流体バイオチップであっても大型の共焦点レーザ誘起蛍光顕微鏡のような巨大な高感度の検出システムを用いて測定しなければならないのが現状である。(図2)コンパクトで高速バイオ分析というマイクロ流体バイオチップの本来の価値を引き出すためには、検出器を含めたシステム全体を小型化する必要がある。このため、産総研では、開発目標として、バイオ分析の中心的な検出方法であり、多様な物質や用例に関する膨大な蓄積データを引き継げる蛍光分析法を選定し、開発してきた。
|
|
 |
 |
|
図2.現状の共焦点レーザ誘起蛍光顕微鏡を用いたマイクロ流体バイオチップ測定システム。大型、レーザと光検出デバイスは非同軸配置のため集積化が難しい。
|
|
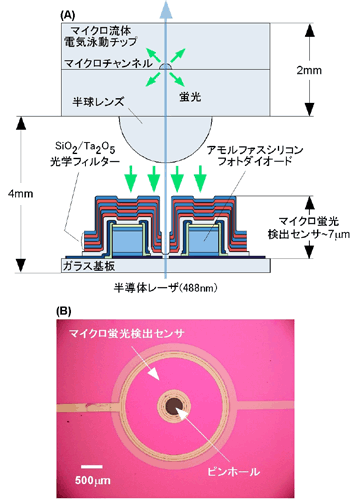
図3.(A)今回開発のマイクロ蛍光検出センサを用いたマイクロ流体バイオチップ測定システムの断面構造。(B)上から見たマイクロ蛍光検出センサの光学顕微鏡写真。レーザと光検出センサは同軸配置、マイクロ流体電気泳動チップに対しては同側配置。励起には半導体レーザを用いた。
|
これまでに、上記のポータブルバイオ分析装置のキーとなる、励起光源と一体化可能な集積型蛍光検出センサを提案・実証し、2003年Analytical Chemistry誌 (Vol. 75, pp. 5300-5305) に発表した。今回は半導体微細加工技術を用いて、アモルファスシリコン・フォトダイオード上に光学干渉フィルターを集積化・パターンニングすることにより、検出限界を下げることに成功した(図3)。なお、本研究開発は、新エネルギー・産業技術総合開発機構の委託事業「Point-of-Care超並列バイオチップを目指した高感度集積型蛍光検出モジュールの研究開発(平成16~18年度)」による支援を受けて行ったものである。また、アモルファスシリコン・フォトダイオードの作製は富士アドバンストテクノロジー(株)が行った。
|
|
|
図4.バイオ分析に使われる色素の蛍光スペクトル帯と結晶シリコンおよびアモルファスシリコンの吸収係数との関係。
(EtBr,TOTO,FAM,EGFPは蛍光色素名)
|
「いい材料は何度も美味しい!」
太陽電池や液晶ディスプレイを駆動する薄膜トランジスタの材料として知られるアモルファス・シリコンはバイオ分析の蛍光検出センサとして理想的とも言える以下の特徴を備えている。
(a) バイオ化学分析に有用な多くの蛍光色素の蛍光スペクトル帯は500 nmから600 nmの可視光領域にあり、この領域でアモルファス・シリコンの吸収係数は結晶シリコンに比べて1桁以上高い(図4)。
(b) 室温で低ノイズ測定が可能であり、冷却装置の必要がなく小型化に有利である。
(c) 200 ℃程度の低温で高品質なアモルファス・シリコンが安価なガラスやプラスチック上に作製でき、低コスト化が容易で量産性に優れている。
「半導体デバイスでは幾何学構造が重要!」
今回、開発したマイクロ蛍光検出センサの大きな特長は、図3(A)に示されているように、励起光源と蛍光検出センサをマイクロ流体電気泳動チップに対して同じ側に、かつ、同軸に配置している点にある。これは、図3(B)に示されているように、可視光に対して透明であるガラス基板上に作製可能なアモルファスシリコン・フォトダイオードと光学干渉フィルターの中央にレーザ光導入のためのピンホールを形成したことにより可能になっている。このような、同側・同軸配置が可能なおかげで、励起光源と蛍光検出センサを集積化したモジュールを形成でき、光軸調整の負担を大幅に低減できる。
「マイクロ蛍光検出センサで高速・高感度・高分解能DNA断片分離に成功」
図3に示されている、マイクロ蛍光検出センサは、半導体微細加工技術によりアモルファスシリコン・フォトダイオード上に厚膜のSiO2/Ta2O5光学干渉フィルターを集積・パターンニングして作製した。マイクロチャンネル中を流れる蛍光色素標識されたサンプルを半導体レーザにより励起し、放出される蛍光をマイクロレンズで収集・並行化し、光学干渉フィルターにより蛍光成分のみを透過させアモルファスシリコン・フォトダイオードにより検出する。このマイクロ蛍光検出センサの性能を、マイクロチャネル中を流れる代表的な蛍光色素フルオレセインの蛍光で評価すると、図5に示すようにその検出限界はフルオレセインの濃度で7 nMであり、その性能は実用レベルに達している。
さらに、マイクロ流体バイオチップによって11種類の長さのDNA断片(制限酵素HaeIIIでφX174バクテリオファージDNAを切断したもの)を電気泳動分離して、その観察に成功した(図6)。検出デバイスも含めて、手のひらサイズの非常にコンパクトなデバイスで、高速(2分程度)、高感度(DNAの検出限界約250pg/µL)、高分解能(理論段数約70000)の電気泳動分離が可能となった。
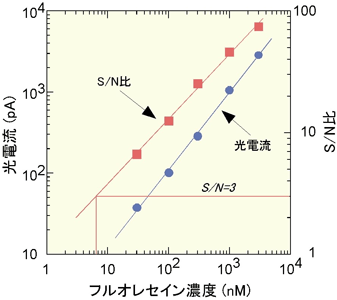
図5.マイクロ蛍光検出センサの光電流およびS/N比のフルオレセイン濃度依存性。
|
|
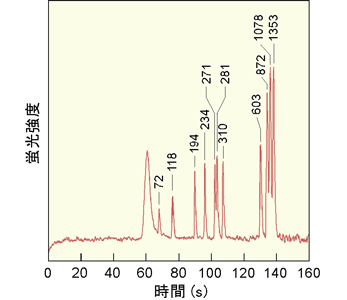
図6.11種類の長さのDNA断片をマイクロ流体電気泳動分離して、マイクロ蛍光検出センサにより検出した。完全な生データ。DNA濃度:100ng/µL。
|
本研究開発は、家庭用DVDドライブ程度の大きさで、DNA、RNA、たんぱく質、糖鎖等の高速分析する装置の原型となるものであり、手術や救急車の緊急医療等、医療処置が必要なその場(Point-of-Care)での高速バイオ分析に道を開くものである。 性能面では検出限界をフルオレセイン濃度で1~2nMまで低減することが当面の目標である。これが実現すれば、さらに高度な分析、例えば、DNAシークエンシングが可能になる。
将来、並列化が容易な青緑色面発光レーザが実現すれば、アモルファスシリコンは200℃という低温プロセスで作製できるので、面発光レーザにマイクロ蛍光検出素子を集積化可能であり、生産性に優れた超並列蛍光検出デバイスが実現できる。このようなデバイスは、DNAシークエンシング等、重要なバイオ分析の桁違いの高スループット化に貢献するものと期待される。