独立行政法人 産業技術総合研究所【理事長 吉川 弘之】(以下「産総研」という)ヒューマンストレスシグナル研究センター【センター長 二木 鋭雄】ストレス計測評価研究チーム 脇田 慎一 研究チーム長、田中 喜秀 主任研究員および永井 秀典 研究員は、SCIVAX株式会社【代表取締役社長 前野 拓道】(以下「SCIVAX社」という)と共同で、産総研が培ってきた最先端のラボチップ(Lab-on-a-Chip)技術を用いて、手軽に、唾液中のストレス関連物質を測るプロトタイプ技術の開発に成功した。
これまで、血液中のコルチゾールやアドレナリンなどの物質が、ストレスマーカー(科学的に根拠のあるストレス指標物質)として提案されていたが、血液測定では採血自体がストレス負荷となり、血管収縮や血圧上昇などが起こり、ストレスが正しく評価・診断できない矛盾があった。
そこで、ストレス負荷を伴わない唾液に注目し、唾液中のストレス関連成分の計測技術を開発してきた。今回は、ストレスマーカーとして最も有力な、唾液中の分泌型免疫グロブリンA(以下「s-IgA」という)とコルチゾール(血液濃度と高い相関性あり)をストレス関連物質に選び、プロトタイプを開発した。
今後、
ヒューマンストレス産業技術研究会の会員の中で、本格的な製品化を目指したアライアンスを構築し、ラボチップの集積化や検出装置の自動化技術を重点開発し、製品開発を目指す。
|
|
|
 |
|
プロトタイプチップとプロトタイプ検出装置
|
厚生労働省の人口動態統計資料によると自殺者数は、平成10年度から毎年3万人前後で推移している。自殺に至る一因である「うつ病」など「ストレス」が原因の「心の病」は深刻な社会問題である。他の病気のように「ストレス」に関して、科学的に根拠のある生体物質(指標物質:以下、「マーカー」という)を、正確に測る技術を開発すれば、「ストレス」の診断・治療のみならず、「心の病」や「自殺」の予防を行う「健康な社会」の実現に資することができる。
また、「ストレス」を客観的に測定評価できれば、食品や創薬の効能評価のみならず、癒し効果や快適性など付加価値の高い商品開発にも有用である。
最近、米国のベンチャー企業が、酵素免疫測定法(以下、「ELISA」という)に基づいたストレス関連物質の測定キットを実用化したものの、1種類の測定に数時間を要するなど、手軽さや正確さにはほど遠い状態である。
産総研ヒューマンストレスシグナル研究センターでは、科学的に根拠のあるストレスマーカーを探索してきた。また、生体試料中のストレスマーカーを迅速、正確に測れるラボチップの開発を行ってきた。さらに、ヒューマンストレス産業技術研究会を発足させ、企業研究者や企画担当者を中心に200名以上の会員を得て、産業ニーズの把握と研究成果の産業技術化を図ってきた。
産総研は、分析スピード向上と試薬量の低減による低コスト化を実現するラボチップ技術に関して、(1)大規模集積化に用いるラボチップの作製研究、(2)ラボチップを利用したストレス計測技術の開発と被験者実験による実証を行ってきた。
ストレスの評価には、唾液中に含まれるストレスマーカーの量を測定するのが有効である。本研究では、ストレスマーカーとして信頼性の高いs-IgAとコルチゾールを測定対象物質に選んだ。しかし、唾液には非常に数多くの生体物質が含まれており、またストレス関連物質は微量であり濃度はたいへん低い(コルチゾールでは数 ng/mL、s-IgAでも100~400 mg/mL)ので、大型の分析機器を駆使しても容易なことではない。
そこで、開発の戦略として、高い選択性を持つ抗原抗体反応を微小な反応場で迅速化し、さらに、電気泳動による高性能分離を組み合わせた分析法をラボチップ上に実現することを考えた。ラボチップ上への集積化により、複数のストレス関連物質を測定することが可能となる。技術的課題は、感度向上と抗体を利用するため高コストになることであった。この課題は、検出装置の高感度化と同時に、対象物質の効率的な濃縮法を組み込んだ、高度な分離分析法を開発することによって解決した。
今回、産総研で開発した要素技術は、(1)プロトタイプチップ、(2)プロトタイプ検出装置、(3)s-IgAとコルチゾールの迅速分析法の開発の3点である。
(1)プロトタイプチップ
チップ内に形成する溝の幾何構造の検討、さらに再現性の良いデータを得るために、コーティングによる表面処理加工、唾液試料の前処理濃縮法、ラボチップへの試料注入や電気泳動分離の流体制御を検討した。これらによって、ラボでの試作レベルで再現性の良い、基礎データを取得できた。
(2)プロトタイプ検出装置
高感度で、しかも選択性の高い検出法として、レーザー励起蛍光法検出器の改良を行った。
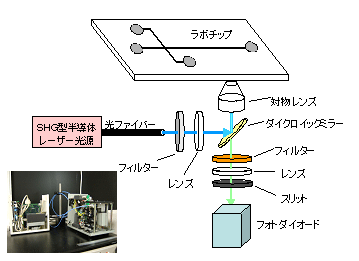
高出力半導体レーザーを用い第2次高調波発生(SHG)素子を使って波長変換し、光ファイバー型の高出力励起光源として用い、蛍光検出光学系の設計・改良研究を行った。
|
|
|
図1 試作したプロトタイプチップと検出システム要素の概要
|
(3)s-IgAとコルチゾールの迅速分析法
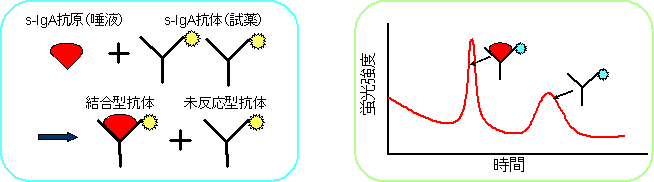
図2に本開発に用いた抗原抗体反応と電気泳動分離による分析原理を示す。唾液中のs-IgA抗原は過剰に存在する蛍光標識抗体(試薬)と完全に結合する。s-IgAと結合した蛍光標識抗体と未結合の蛍光標識抗体(試薬)は分子量の差が大きいので容易に電気泳動により分離できて、レーザー光を使い高感度に蛍光検出する。図3に得られたデータと検量線を示す。
 |
|
図2 本分析法の原理図(左:抗原抗体反応、右:電気泳動による分離)
唾液中のs-IgAは蛍光標識抗体と特異的に結合し、結合型と未反応型抗体を電気泳動速度の違いで分離
|
|
|
|
図3 得られたs-IgAの検出データと検量線(理論フィット)
|
一方、コルチゾール分析では、唾液中に蛍光標識化コルチゾール標品を加え、抗体に結合していない未反応の蛍光標識化コルチゾール標品を電気泳動分離して蛍光検出し、唾液中のコルチゾールを測定する方法を開発し、s-IgAと同様に検量線を得た。
s-IgAとコルチゾール分析のどちらも、電気泳動分離・検出に必要な時間は3分以内であり、迅速な分離分析を達成することができた。
ラボチップの集積化や装置自動化による製品プロトタイプを開発する企業との連携を希望している。今後、ヒューマンストレス産業技術研究会の会員に呼びかけ、高い技術水準を持つ研究開発セクターとアライアンスを構築し、さらに、ラボチップ技術の集積化や自動化を展開することにより、(1)複数の測定項目を、(2)誰でも手軽に測定できる製品開発を行いたい。