独立行政法人産業技術総合研究所【理事長 吉川 弘之】(以下「産総研」という)単一分子生体ナノ計測研究ラボ【ラボ長:馬場嘉信 名古屋大教授】のルミアナ・バカロヴァ研究員と大庭英樹主任研究員は、がん細胞を特異的に識別できるレクチンと量子ドットと呼ばれるナノ材料とを融合させた新規材料を開発し、この新規材料が、がん治療に応用できる可能性を世界に先駆けて明らかにした。この成果は、アメリカの科学誌Nature Biotechnologyの11月号4日号に掲載された。
量子ドットは、半導体の無機材料でできた数nmの粒子状の物質であり、紫外線をあてると強い蛍光を出すところから(図1)、細胞内の遺伝子・タンパク質や生体内のがん細胞をイメージングできる材料として世界的に注目を集め、熾烈な研究開発競争が展開されている。同ラボにおいては、この量子ドットを簡便に合成する手法と量子ドットとがん細胞を識別できる抗体やレクチンを融合させた材料を合成する手法を新たに開発し、簡便に正常細胞とがん細胞を識別できる技術を開発した。さらに、量子ドットが選択的に結合したがん細胞に紫外線を照射するだけで、がん細胞が死んでしまうことを発見し、量子ドットが分子イメージングだけでなく、がんの治療にも応用可能であることを世界で初めて明らかにした。
合成した量子ドットは、セレン化カドミウム(CdSe)という材料で、直径は、わずか3 ナノメートル(10億分の1メートル)しかない(図2左)。量子ドットに紫外線を照射すると、非常に鮮やかな緑色(図2右)の蛍光を発する。量子ドットは、優れた材料であるが、タンパク質などの生体分子とは適合性が悪い材料であり、これまでバイオテクノロジーへの応用は限られていた。本研究においては、量子ドットにタンパク質を融合させる新規技術を開発し、がん細胞の表面にある糖鎖を特異的に認識するレクチンと量子ドットを融合した材料を開発することに成功した(図3)。この材料をがん細胞に与えて、紫外線を照射すると、がん細胞の表面や内部に量子ドットが結合して鮮やかな緑色の蛍光を発する(図4, 5)。これに対して、この材料を正常細胞に与えても、正常細胞には作用しないために、全く蛍光を発しない(図5)。この技術は、このように、がん細胞と正常細胞を簡便・正確に識別することに応用できる。

図1 量子ドットが発する蛍光
量子ドットに紫外線をあてると、サイズが小さい(2ナノメートル)と青色の蛍光を発し、3ナノメートルでは緑色、4ナノメートルでは黄色、5ナノメートルでは赤色の蛍光を発する。
|
|

図2 合成した量子ドットの電子顕微鏡写真(左)と量子ドットが発する蛍光(右)
今回は3ナノメートルの量子ドットを合成した。右図の左側は紫外線照射前の量子ドット溶液、右側は紫外線照射時。
|
 |
|
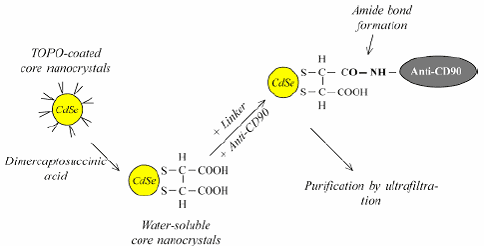
図3 量子ドットとレクチンを融合して新規材料を作成する方法 |
|
|
図4 量子ドットとレクチンの融合材料が病態細胞内に取り込まれる経過の観察結果
上段:1時間後の蛍光画像(左)と透過観察像(右)
下段:5時間後の蛍光画像(左)と透過観察像(右)
融合材料は細胞表面に集まるとともに、一部細胞内にも入っている。 |
|
|
図5 量子ドットとレクチンの融合材料によるがん細胞(左)と正常細胞(右)の識別
がん細胞のみ選択的に蛍光を発している。 |
さらに、これらの細胞に紫外線を照射し続けると、紫外線の強度にも依存するが、10分後には、がん細胞だけが死に始めることが分かった。さらに、紫外線照射後60分で、がん細胞全体の10から15%が死んでしまうことが明らかとなった。同様な実験を正常細胞で行っても、細胞は全く死ななかった。様々な実験を追加して行った結果、このメカニズムは下記のように推定された。量子ドットとレクチンが融合した材料では、レクチンが細胞表面に結合することで、がん細胞表面にのみ量子ドットが存在する。そこに、紫外線が照射されると量子ドットは紫外線のエネルギーを吸収して蛍光を発する。しかし、吸収されたエネルギーの一部は、量子ドット付近に存在する酸素と反応して、活性酸素や1重項酸素などの生体にとって有毒な酸素種を発生させる。これらが、がん細胞にアポトーシス(細胞死)を誘導し、殺してしまうこと考えられる(図6)。詳細な実験結果は、アメリカ化学会のナノテクノロジー専門誌(Nano Lett.)9月号に掲載された。
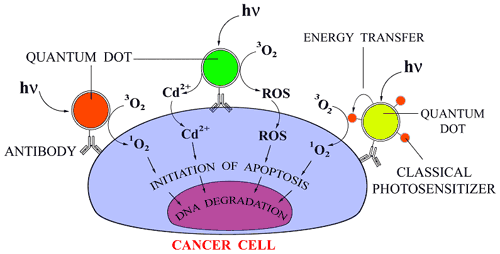 |
図6 ナノ材料ががん細胞にアポトーシス(細胞死)を起こすメカニズム
量子ドットとレクチンの融合材料ががん細胞表面に結合し、紫外線を照射すると活性酸素が発生し、細胞死を誘発する。 |
これらの実験結果は、細胞レベルの実験であり、今後、動物実験や臨床試験を積み重ねていくことが重要であり、実際の臨床応用には、まだ課題が多いが、量子ドットのようなナノ材料が、がん治療にも応用可能であることを、世界で初めて示した意義は大きい。
フォトダイナミック療法(光線力学的療法:PDT)は、光感受性薬剤とレーザー光によって引き起こされる光化学反応を利用した治療法で、腫瘍組織中に活性酸素を生成させ、その力によって腫瘍組織を死滅させるものである。具体的にはあらかじめ罹患者に薬剤を静注し、腫瘍組織と正常組織における薬剤の濃度の差が最大となる48~72時間後に薬剤の励起波長と一致する波長の低出力レーザー(エキシマレーザー)光を照射する。この際、使用するレーザーは、レーザーメスの約1/100と低出力な上、薬剤は、腫瘍組織に多く集積するため正常組織への障害を最小限に抑え、がん病巣のみを選択的に治療することができるため、がんの画期的な治療法と期待されている。ところが、 Trifluoperazine (TFPZ) や Sulfonated Aluminum Phtalocyanine (SALPC) なども光感受性薬剤として知られているが、現在のところPDT用に市販・使用されている光感受性薬剤は、ポリフィマーナトリウム(商品名フォトフリン)のみで、これらに代わる、新規な光感受性薬剤の開発が望まれている。
産総研・単一ラボは量子ドットと呼ばれる、半導体の無機材料でできた数nmの粒子状の物質を簡便に合成する手法と量子ドットとがん細胞を識別できる抗体やレクチンを融合させた材料を合成する手法を新たに開発し、既に簡便に正常細胞とがん細胞を識別することに成功している。さらに、量子ドットの新たな機能探索と展開を目指して、下記の研究を行った。
量子ドットをガン細胞と特異的に結合する物質である抗体と融合させたものをガン細胞に添加して、紫外線を照射し続けると、紫外線の強度にも依存するが、10分後には、ガン細胞だけが死に始めることが分かった。さらに、紫外線照射後60分で、ガン細胞全体の10から15%が死んでしまうことが明らかとなった。この系にTFPZやSALPCを共存させると、この死滅効果が増すことが明らかとなった。同様な実験を正常な細胞で行っても、細胞は全く死ななかった。
CdSe以外の量子ドットについても同様に検討すると共に、融合させる抗体やレクチンの種類を変えることにより、固形ガンから白血病などの血球細胞の幅広いガンに対応できる光感受性薬剤の開発を目指す。