独立行政法人 産業技術総合研究所【理事長 吉川 弘之】(以下「産総研」という)電力エネルギー研究部門【部門長 大和田野 芳郎】は、規則正しく整列したナノ細孔を有する三次元構造を備え、かつ細孔を形作るフレームワークが結晶性金属酸化物である結晶性金属酸化物複合ナノポーラス材料(結晶性金属酸化物複合多孔質材料)の合成に世界で初めて成功した。

高い比表面積を有する三次元構造を持つ微結晶TiO2-P2O5複合ナノポーラス粉末の透過電子顕微鏡写真
|
本材料は結晶金属酸化物の電子的あるいは化学的機能とナノ細孔の分子ふるい機能を活かして、触媒担体、吸着剤、光触媒、湿式太陽電池、センサー、エネルギー貯蔵デバイスなどへの応用が期待される。
金属酸化物ナノポーラス材料(金属酸化物多孔質材料)は、1995年に米国Massachusetts工科大学(MIT)の研究グループによって開発され、三次元的に規則正しく整列したナノサイズ細孔や、高比表面積などを有することで注目されているが、細孔を形作るフレームワークが、化学的に安定なアモルファス(結晶でない固体)だったため、結晶が有している規則的な原子配列に基づく様々な電子的あるいは化学的機能を利用することができなかった。世界中の研究グループがフレームワークを結晶相で作ることに取り組んできたが、ナノオーダーで金属酸化物を結晶成長させると結晶の大きさが制御できず、三次元的に規則正しく整列した構造が潰されてしまうため、現在まで成功した例がなかった。
通常、金属酸化物ナノポーラス材料の製造にはテンプレート(鋳型)を使用した合成法が用いられるが、産総研は新しい着想から、従来の合成法にガラス相の前駆体であるトリエチルリン酸[PO(OC2H5)3]又はオルトケイ酸テトラエチル[Si(OC2H5)4(TEOS)]を微量加え、高温焼結で金属酸化物の結晶化を制御しながら成長させることで、規則正しく整列したナノ細孔を有する三次元構造を備え、フレームワークが結晶性金属酸化物であるナノポーラス材料の合成に成功した。また、ガラス相に、イオン性や電子電導性などの性能を持つ機能性物質のドープが可能であり、多様な物質に適用が可能である。
さまざまな結晶性金属酸化物のもつ電子的・化学的機能とナノポーラス構造のもつ分子サイズのふるい機能を組み合わせることが可能となったので、触媒担体、吸着剤、光触媒、湿式太陽電池、センサー、エネルギー貯蔵デバイス等幅広く適用できると期待される。なお、本件は特許出願中である。
※本研究成果は、英国科学誌 Nature Materials 2004年1月号に掲載された。
構造中に分子レベルの細孔を有するナノポーラス材料は、吸着剤、触媒担体、分離膜、生体分子或いは金属や半導体クラスターの固定剤、機能性エレクトロニクス材料やフォトニクス材料などへの応用が期待されている。そのためには、均一な細孔のサイズ、形状、孔の配向に秩序構造を持つ物質が望ましい。これらの特徴を備える天然ナノポーラス物質にはゼオライトがあるが、天然ゼオライトの孔径は1.2nm以下であり、その孔径により用途が限定されるため、より広い領域に応用するためには、孔径がより大きく、かつ細孔配向の揃った物質が求められている。
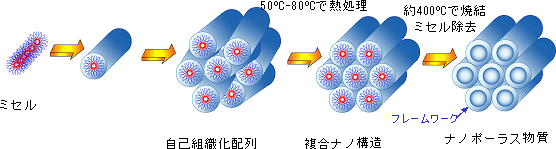
1990年に早稲田大学の研究グループが層状ケイ酸塩へイオンの層間挿入反応と熱処理により、また、1992年に米国Mobil社が界面活性剤を鋳型とした水熱反応法により、均一なナノ細孔が蜂の巣状のように配列した構造を有するナノポーラスシリカ(二酸化ケイ素)の合成を報告した。【図1】に米国Mobil社が用いた鋳型法を示す。これらのナノポーラス材料は、2nm以上の孔径を有し、均一な細孔サイズ、高比表面積、多種多様な三次元細孔構造(例えば:六方、立方、層状)などの特徴を有しているため注目され、この報告以来、界面活性剤を鋳型としたナノポーラス材料の研究が注目された。特に、光触媒や機能性電子部品や光機能部品など広い範囲へ応用の可能性があるナノポーラス金属酸化物を次のターゲットとした研究が盛んに行われてきた。
|
|
|
図1 鋳型法を用いる、ナノポーラス材料合成プロセス
|
1995年に米国Massachusetts工科大学(MIT)の研究グループによって、三次元的に規則正しく整列したナノサイズ細孔や、高比表面積などを有する金属酸化物ナノポーラス材料が開発された、しかし、フレームワークが化学的に安定なアモルファス(結晶でない固体)だったため、結晶が有している規則的な原子配列に基づく様々な電子的あるいは化学的機能を利用することができなかった。世界中の研究グループがフレームワークを結晶相で作ることに取り組んできたが、ナノオーダーで金属酸化物を結晶成長させると、結晶の大きさが制御できず、三次元的に規則正しく整列したナノ細孔構造が潰されてしまうため、現在まで成功した例がなかった。
通常、金属酸化物ナノポーラス材料の製造には、テンプレート(鋳型)を使用した合成法が用いられるが、産総研は新しい着想から、従来の鋳型合成法に、ガラス相の前駆体であるトリエチルリン酸[PO(OC2H5)3]又はオルトケイ酸テトラエチル[Si(OC2H5)4(TEOS)]を微量加えることにより合成プロセスを改善した。
|
|
|
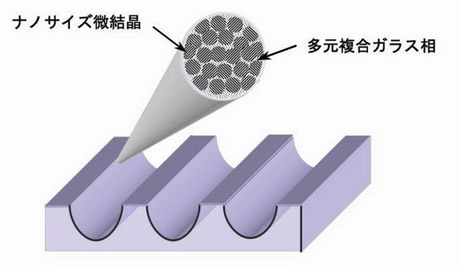
図2 高い比表面積を有する三次元構造を持つ微結晶金属酸化物複合ナノポーラス材料のイメージ像。
|
具体的な合成法としては、まず鋳型としてのブロック高分子をエターノールに溶かしてミセルを形成させる。次に金属アルコキシド[例えば:テトライソプロピルチタンTi(OC3H7)4或いはテトライソブチルオキシジルコニウムZr(OC4H9)4等] 或いは塩化金属[例えば:塩化ニオブNbCl5, 五塩化タングステンWCl5など]とトリエチルリン酸[PO(OC2H5)3]を添加し、更に塩酸[HCl]を加え、ミセルの鋳型の上に加水・縮重合などのゾル-ゲル法によりゲル化させ、ガラス相である五酸化リン[P2O5]-金属酸化物が共存した複合ナノ構造を有する材料を合成する。数日間低温60-80℃で処理し、それから空気中350-400℃で数時間加熱処理することによってブロック高分子を除去し、微量のガラス相である五酸化リン[P2O5]を含む金属酸化物ナノポーラス材料を合成する。この時点ではナノオーダーでアモルファス金属酸化物とガラス相である五酸化二リン[P2O5]が共存している。更にこれを金属酸化物の相転移温度を越える温度領域400-700℃で熱処理することによって、アモルファスの金属酸化物を微結晶に相転移させる。この温度領域は、五酸化二リン[P2O5]はガラス相のまま安定な状態で存在できるが、金属酸化物にとっては、相転移点を越えるため、結晶核を結成する。この時安定なガラス相である五酸化リン[P2O5]が金属酸化物の微結晶の間に入り、微結晶の過大成長を防ぎ、かつ接着剤の役割を果たして、一個一個ブロックのような4-6nmの微結晶を繋ぎ、規則正しく整列した微結晶を有する金属酸化物複合ナノポーラス材料の構築が可能となる【図2参照】。この材料は、均一な細孔(約4nm)とフレームワーク幅(約5nm)、高比表面積(約200-300m2/g)、耐熱性などの特徴を有する。また、微結晶のサイズは、熱処理温度による制御することが可能である。
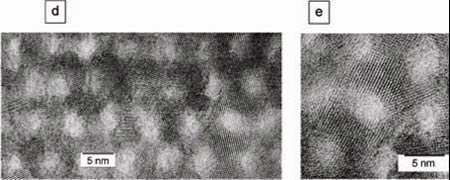
この新規手法によりガラス相として五酸化二リン[P2O5]や二酸化ケイ素[SiO2]を用い、さまざまな金属酸化物(例えば、酸化チタン[TiO2]、酸化マンガン[MnO2]など)を組み合わせることにより、高い比表面積を持つ、ナノサイズ微結晶で構成された種々の金属酸化物-ガラス相複合ナノポーラスの合成にも成功している。【図3】に、TiO2-P2O5とTiO2-P2O5-MnO2の高分解透過電子顕微鏡の写真を示す。
更に、ガラス相五酸化二リン[P2O5]は目的に応じ、材料の電子伝導性或いはイオン伝導性を改善するために、イオン性や電子電導性などの性能を持つ機能性物質をドープすることが可能である。
|

|
 |
|
図3 三次元構造的微結晶酸化物のフレームワークを有するナノポーラス粉末の透過電子顕微鏡(TEM)写真である。
(a)、(b)と(c)はTiO2-P2O5のTEM像、(d)と(e)はTiO2-P2O5-MnO2のTEM像
|
本合成プロセスは、無機・有機複合材料の典型的な合成法である鋳型法と、構造セラミクス機能材料に用いられる焼結法とを組み合わせたものであり、自己組織化ナノポーラス材料と機能性セラミクスとの融合を実現した。今後は様々な金属酸化物のもつ電子的・化学的機能とナノポーラス構造のもつ分子サイズのふるい機能を組み合わせることが可能となり、触媒担体、吸着剤、光触媒、湿式太陽電池、センサー、エネルギー貯蔵デバイス等に幅広く適用できると期待される。次の展開としてデバイス化のために必要な高性能な薄膜作製を本手法により合成する研究開発を行っている。