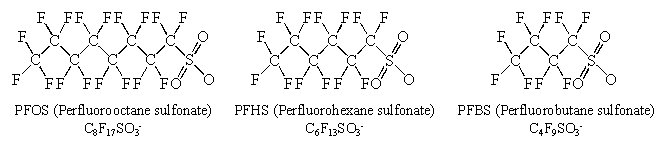 |
|
Figure 1 Structures of perfluoroalkane sulfonates |
地球温暖化ガス問題・残留性有害化学物質(いわゆるPOPs)問題の解決は21世紀の地球環境保全技術の双璧をなす研究領域であるが、両者における共通課題としてクローズアップされているのが人工フッ素有機化合物問題である。従来、フロンに代表される揮発性人工フッ素有機化合物に関しては、膨大な国家予算を費やし無数の研究がなされてきたが、難/半揮発性の残留性人工フッ素有機化合物に関する研究はほとんどなされていない。
日本国内が環境ホルモン問題で右往左往していた2000年5月、米国3M社は年間約3億ドル以上の減収にもかかわらず、PFOS (perfluorooctane sulfonate、パーフルオロオクタンスルホン酸塩)の使用中止を発表した。PFOSが高濃度で人や生物に蓄積し、広く環境中に残留していることが明らかになったためである。PFOSとはフッ素を含んだ人工有機フッ素化合物で、これからフッ素系のコーティング剤・界面活性剤・難燃剤等の関連化合物が合成される。特にコーティング剤としては家具・建築材や衣類等、多用途に莫大な量が過去数十年に渡り使用されてきた。
PFOS関連化学物質については、過去2年間で25報以上の論文が国際誌に発表されているように、国外では非常に活発な研究活動が行われているのに対し、国内では平成12年度NEDO即効型産業技術研究「PFOS 関連物質の分析法確立・危険性評価に関する研究」以降、平成15年度地球環境研究推進事業「PFOS類の海洋環境動態研究手法の開発に関する予備的研究」が開始されるまで、ほとんど研究がなされていなかった。唯一、Kannan博士による国内血液試料の分析例があるが、現在まで国内汚染状況を把握する知見に乏しいため、本研究では日本におけるPFOS関連物質の「汚染マップ」作成と、リスク評価の必須情報である「生物濃縮係数 (BCF) : bioconcentration factor」の算出を試みた。
本稿は最近の研究発表、ダイオキシン国際会議(Dioxin 2002, Barcelona, Spain, 2002)、ORGANOHALOGEN COMPOUNDS, 59, 311-314, 2002、日本分析化学会年会(札幌,2002)、平成12年度NEDO即効型産業技術研究報告「PFOS 関連物質の分析法確立・危険性評価に関する研究」、環境ホルモン学会第5回研究発表会(広島, 2002)、SETAC-Europe (Hamburg, 2003), PFOA Workshop (Hamburg, 2003)他の一部を抜粋したものである。
2000年-2002年にかけて、全国主要水域の魚類、鳥類(一部哺乳類)および海水・淡水中PFOS関連物質の残留量を調査した。その結果、東京湾の魚全てから血液中濃度2~489ng/mL、肝臓中濃度37~558ng/g-wetの範囲でPFOSが検出された。これらの濃度はほとんどPCB濃度と同程度で、ダイオキシン(PCDD/PCDF)よりも1万倍以上高濃度であった。また、魚血液中濃度は人血液よりも10倍以上高く、ダイオキシンとは異なった生物濃縮メカニズムを有することが判明した。また、東京湾海水中PFOS濃度は8~59ng/Lであり、PCBやダイオキシン類とは桁違いに高濃度であり、むしろ多環芳香族炭化水素の汚染状況と比較可能な程度であった。また、東京湾における生物濃縮係数(BCF)を計算したところ、魚種ごとに差があるが1400~21,000で、ダイオキシン類と同程度の蓄積性を有することを明らかにした。このBCF値はMoody11)による実験室データと一致し、実環境試料でのBCF値を初めて算出することができた。
またここでは詳細は省略するが、鳥類についてはガン・カモ類とカラスで濃度差が認められ食性を反映していると推測される。
本研究結果より、PFOS関連物質による環境汚染が国内でも広範囲に生じ、また生物濃縮のメカニズムが他のPOPsとは異なることが示唆された。これについては胆汁循環を生物濃縮の一因とする室内実験データと一致する。
PFOSの半数致死量(LD50)はラットで250mg/kg、血清NOAEL(無毒性量)は50ppm前後と報告されているため、ここで明らかになった人血を含む生物試料中濃度はいずれも生物個体に障害を生じるレベルではない。
ここで注意するべきなのは、PFOS関連化学物質の特異性は、毒作用ではなく、その残留性と環境動態にある点である。特に、ダイオキシンなど有機塩素化合物と比較しても極端に難分解性(硫酸で24時間煮沸しても安定)であり、これは炭素-フッ素の強い共有結合に起因している。さらに、安定した炭素-フッ素骨格の無極性(水に溶けにくい)分子の末端に極性(水に溶けやすい)の分子構造をもつため、界面活性剤的な性質を持ち、水に溶け難く脂溶性の高いダイオキシン類とは生物濃縮メカニズム・環境内挙動が異なると推測されている。これは本研究で水環境中に高濃度で存在することが明らかになった結果と一致する。さらに末端の極性分子が化学修飾され、揮発性と極性の異なる関連化合物が多数存在することで、この種の残留性人工フッ素化合物の環境動態には輸送・環境内化学構造変化・蓄積現象等の複雑な相互作用が影響していると考えられる。
以上、残留性人工フッ素化合物問題については、リスク評価の不備によりダイオキシン問題を内在した塩素系化学産業と同じ状況を防ぐためにも、その環境内運命(どこから来て、どこへゆくのか)と危険性を早急に解明し、適切なリスク評価を行うことが緊要である。
下記に、補足データを記載する。
MATERIALS & METHODS
Blood and Liver of bird, fish, surface seawater and human blood were analyzed in this study. Forty four blood and eleven liver samples of fish and thirteen surface sea water samples were analyzed and these were collected from Tokyo Bay, Osaka Bay, Lake Biwa, Seto Inland Sea, Ariake Bay, and Okinawa in Japan (Figure 3) during March-June, 2002. Human blood and sera were collected from Japanese citizens (n=3, age: 25~36) in June, 2002. Extraction procedures for blood, liver and water are presented elsewhere15).
RESULTS & DISCUSSION
Contamination of PFOS in Japan
◇ PFOS was found in blood and livers of all fishes and surface water from Japan.
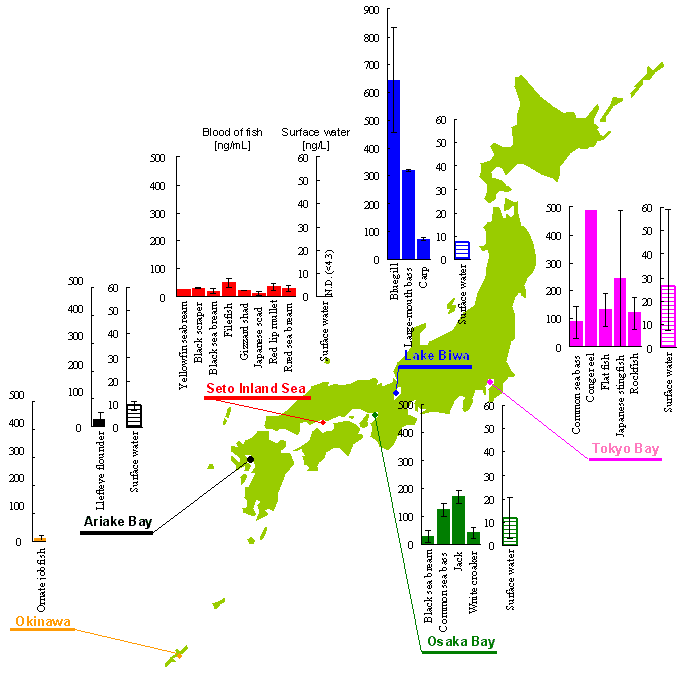
◇ Concentrations of PFOS in blood of fishes ranged from 2 to 834 ng/mL, and in the order of
Lake Biwa (Ave.=345ng/mL)> Tokyo Bay (172) > Osaka Bay (100) > Seto Inland Sea (29) > Ariake Bay (28) > Okinawa (10).
◇ The greatest concentration PFOS in surface water was found in Tokyo Bay at 59 ng/L, and in the order of
Tokyo Bay (Ave.=26ng/L) > Osaka Bay (12)> Ariake Bay (9.0)> Lake Biwa (7.4) > Seto Inland Sea (<4.3).
◇ PFHS was detected in some fishes and surface water samples.
◇ The greatest concentration of PFHS was found 121ng/mL in blood of flat fish from Tokyo Bay.
◇ PFBS was not found in any samples.
 |
|
Figure 3 Spatial distribution of PFOS in fish [ng/mL] and surface water [ng/L] from Japan.
|
Comparison PFOS with the other pollutants in Japan
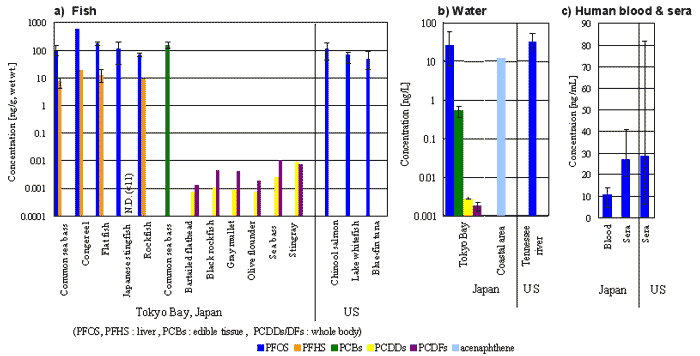
◇ Concentrations of PFOS in blood of fishes were comparable to those of PCBs and 10,000 times higher than those of PCDDs and PCDFs.
◇ Concentrations of PFOS in surface water were similar to those of PAH and much more higher than those of PCBs, PCDDs and PCDFs.
◇ PFOS concentrations in blood of fishes were approximately 10 times higher than those in Japanese human blood.
Comparison Japan with US
◇ Concentrations of PFOS in Japanese fishes were similar to those in some fishes from the Great Lakes region of the US.
◇ Concentrations of PFOS in surface water of Tokyo Bay were similar to those reported for the Tennessee River in the US.
◇ PFOS concentrations in Japanese sera were similar to American.
 |
|
Figure 4 Concentrations of perfluoroalkane sulfonates and the other pollutants in Japan and US 3),4),7)~10).
|
Bioconcentration Factor (BCF) of PFOS in fish
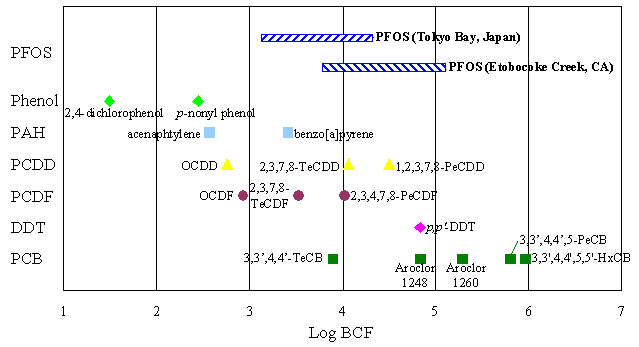
◇ Log BCF of PFOS ranged from 3.1 to 4.3 in Tokyo Bay.
◇ BCF of PFOS was similar to those of PCDDs and PCDFs.
◇ BCF of PFOS in Tokyo Bay was similar to or less than those in Etobocoke Creek, a contaminated area in the Canada.
These results provide the first evidence of occurrence of PFOS in fishes, surface water and human blood in Japan and that the concentrations are comparable to those in the US. Of the three perfluoroalkane sulfonates monitored, PFOS was the most predominant fluorochemicals in the tissues analyzed. The situation of PFOS pollution in Japan supposes to be similar to those of PCBs and/or PAHs. Quantitative bioaccumulation of PFOS in fish from surface water was made clear in this study. Considering the necessity to perform comprehensive survey of PFOS and related compounds to understand the mechanisms of human exposure and environmental fate of PFOS in Japan, the second national research project "Development of comprehensive risk database for PFOS related compounds" will start in 2003 by AIST(EMTECH) and NIAH supported by Ministry of Environment.
REFERENCES
1) B. D. Key et al. Environ. Sci. Technol. 1997, 31, 2445-2454
2) G. W. Olsen et al. J. Occup. Environ. Med. 1999, 41, 799-806
3) K. J. Hansen et al. Environ. Sci. Tecnol. 2001, 35, 766-770
4) J. P. Giesy et al. Environ. Sci. Technol. 2001, 35, 1339-1342
5) K. Kannan et al. Environ. Sci. Technol. 2001, 35, 3065-3070
6) K. Kannan et al. Environ. Sci. Technol. 2002, 36, 2566-2571
7) Environment Agency JAPAN Chemicals in the Environment 2000 2001
8) T. Sakurai et al. Chemosphere 2000, 40, 627-640
9) K. J. Hansen et al. Environm. Sci. Tecnol. 2002, 36, 1681-1685
10) N. Yamashita et al. Organohalogen Compounds 1998, 39, 389-392
11) C. A. Moody et al. Environ. Sci. Technol. 2002, 36, 545-551
12) X. Lu et al. Chemosphere 2000, 41, 1675-1688
13) R. W. Gale et al. Environ. Sci. Technol. 1997, 31, 178-187
14) D. Mackay Environ. Sci. Technol. 1982, 16, 274-278
15) S. Taniyasu et al., ORGANOHALOGEN COMPOUNDS, 59, 311-314, 2002