材料科学と免疫学を応用した新規がんワクチンの開発
免疫増強作用があるメソポーラスシリカ(MS)ナノ粒子の表面に、抗原と免疫賦活分子を組み込んだ有機金属構造体(MOF)を形成し、新規がんワクチンを作製した。MOFが抗原や免疫賦活分子を保護するとともに放出を制御することを狙っている。このがんワクチンを、免疫チェックポイント阻害剤である抗PD-1抗体と併用すると、免疫ブレーキをOFFにする抗PD-1抗体と免疫アクセルをONにするワクチンとの相乗効果が生まれ、担がんマウスにおいて抗PD-1抗体の必要投与量を1/10に削減できた。
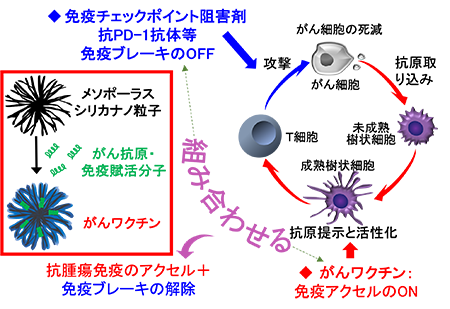 がんワクチンとチェックポイント阻害剤の相乗効果
がんワクチンとチェックポイント阻害剤の相乗効果
免疫チェックポイント阻害剤の問題点と克服策
免疫チェックポイント阻害剤は、がん細胞によって抑制されていた免疫機能を再び活性化させるもので(免疫ブレーキのOFF)、がん免疫療法の可能性を広げた。しかし、奏効率は10~40 %にとどまるとともに、非常に高価であることと、過剰な免疫ブレーキOFFに伴う免疫関連の副作用が問題となっている。これを克服するため、がんワクチン等の免疫アクセルを併用する複合免疫療法が提案されている。本研究では、抗原や免疫賦活分子を効果的に保持できるとともに放出制御が期待できる「有機金属構造体ゲート化メソポーラスシリカ(MS@MOF)」で、がんワクチンを構成することを目指した。
階層的自己組織化、マウスを用いたin vivo試験
MS@MOFの自己組織化条件を検討し、がん抗原や免疫賦活分子の組み込み条件を最適化した。その結果、モデルがん抗原であるオバルブミン(OVA)、免疫賦活分子であるポリイノシン酸-ポリシチジル酸、チェックポイント阻害剤である抗CTLA-4抗体など、様々な巨大分子をMS@MOFに階層的に組み込むことができた。またMS@MOFはpHによって分解のしやすさが異なることを確認した。特に、中性条件下ではMS@MOFの分解が遅く、酸性条件下(pH5)では迅速に分解されることは、抗原や免疫賦活分子の早期放出を防ぎ、細胞内への送達を促進するのに有利である。マウス実験では、MS@MOFがんワクチンの皮下投与とチェックポイント阻害剤である抗PD-1抗体の全身投与の併用によって抗腫瘍免疫が活性化され、抗PD-1抗体の必要投与量は抗PD-1抗体の単独投与に比べて1/10に削減できた。また安全性評価として、MS@MOF皮下投与後の肝機能、腎機能、および肝臓、腎臓、脾臓、心臓、肺の各組織への影響を調べたところ、明らかな毒性は観察されなかった。
 MS(左)とMS@MOF(右)粒子のTEM写真
MS(左)とMS@MOF(右)粒子のTEM写真
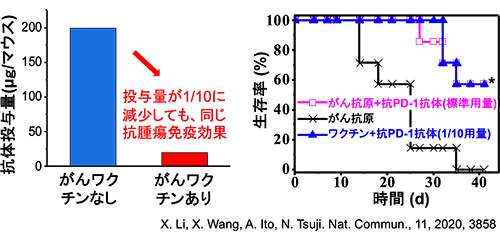 がんワクチンの利用による抗PD-1抗体の投与量削減
がんワクチンの利用による抗PD-1抗体の投与量削減
幅広い応用の可能性と橋渡し研究
開発した無機・有機複合ナノ材料の送達システムは、タンパク、核酸、化学療法薬等、さまざまな治療薬に広く応用できると期待される。本研究はマウスを用いたものであり、この技術を臨床応用するためには、試験研究から臨床研究に至るまで一気通貫した研究がさらに必要であり、ヒトにおける安全性と有効性を実証するためには臨床試験が必要である。
ご協力・ご助言をいただいた共同研究者、連携研究者に深く感謝いたします。
本研究は産総研, JSPS 科研費JP22H03964, JP17K01399, JP26750162, JP23700567の助成を受けたものです。データの一部は下記の論文から引用。
Xia Li, Xiupeng Wang, Atsuo Ito, Noriko M. Tsuji. A nanoscale metal organic frameworks-based vaccine synergises with PD-1 blockade to potentiate anti-tumour immunity. Nature Communications. 2020; 11: 3858